Capitolul 2: Factorul asemănător Krϋppel 15 suprimă proliferarea celulelor glomerulare mezangiale renale prin îmbunătățirea conjugării P53 SUMO1
May 12, 2022
Pentru mai multe informatii. a lua legaturatina.xiang@wecistanche.com
3. REZULTATE
3.1|Depistarea genelor de legare KLF15-prin ChIP-Seq în MC glomerulare renale primare
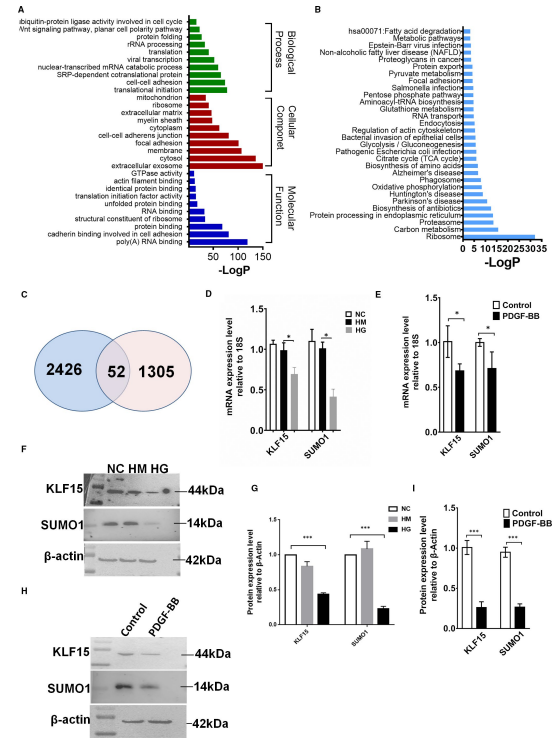
Pentru a identifica genele partenere de legare directă ale KLF15, am efectuat analiza ChlP-Seq și, în cele din urmă, am analizat 2478 de gene. Analiza GO a acestor gene prin intermediul instrumentului de pe site-ul web www.uniprot.org (Figura 1A, B) a dezvăluit termeni de funcție moleculară asociați cu 1941 de gene, termeni de componente celulare legați de 1662 de gene și termeni de proces biologic legați de 1766 de gene. Deoarece scopul nostru a fost să aflăm cum KLF15 afectează MC-urile, ne-am concentrat pe genele legate de procesele celulare. Dintre cele 1315 gene legate de procesele celulare, s-a descoperit că 74 de gene participă la procesele ciclului celular; în mod specific, aceste gene au participat la ciclul celular mitotic, la tranziția de fază a ciclului celular și la alte procese (Figura 1C, D). În plus, am analizat genele implicate în creștere și am constatat că acestea sunt legate de creșterea dezvoltării, creșterea celulelor și alte tipuri de creștere (Figura 1E).

3.2|Depistarea genelor reglate diferențial în MC-uri glomerulare renale care supraexprimă KLF15- folosind SILAC și LC/MS
Analiza SILAC și LC/MS a HRMC-urilor care supraexprimă KLF15 în comparație cu celulele parentale a condus la identificarea a 1357 proteine. Am folosit DAVID și IPA pentru a achiziționa domeniile GO și căile îmbogățite ale proteinelor cuantificate identificate de SILAC. În mod interesant, mulți termeni legați de funcția biologică ai proteinelor s-au numărat printre primii 30 de termeni GO semnificativ îmbogățiți, inclusiv reglarea procesului metabolic al aminoacizilor celulari, complexul proteazomului, legarea proteinelor și termenii de transcripție și traducere, toți fiind strâns legați de ubiquitinare (Figura 2A). Figura 2B prezintă primii 30 de termeni de cale semnificativ îmbogățiți. Mai mulți termeni de proces biologic, inclusiv termenii proteazom și boli neurodegenerative, au fost, de asemenea, legați de ubiquitinare.

Faceți clic pentru a afla desprecistanchede vanzare cu detalii
3.3|Analiza bioinformatică a genelor de legare KLF15-care sunt potențial asociate cu proliferarea MC glomerulară renală
Pentru a explora genele de legare KLF15-care sunt potențial asociate cuglomerular renalProliferarea MC, am efectuat o analiză bioinformatică a datelor ChIP-Seq și a datelor SILAC-LC/MS. Au fost verificate cincizeci și două de gene (Tabelul 2 și Figura 2C) și cinci dintre aceste gene, inclusiv SUMO1, factorul inhibitor al migrației macrofagelor (MIF), factorul de inițiere eucariotic (EIF), factorul de creștere asemănător insulinei (IGF) și reticulocalbin (RCN). ), erau strâns legate deproliferarea celulară. Deoarece analizele GO și ale căilor proteinelor exprimate diferențial au sugerat că genele ecranate au fost legate în principal de procesul de ubiquitinare, am ajuns la concluzia că SUMO1, un membru al familiei de proteine de tip ubiquitin-like (UBL), participă la modificarea post-translațională similară cu ubiquitinarea ca genă țintă a KLF15.
Un număr tot mai mare de dovezi au indicat că HG este unul dintre factorii majori care induc dezvoltarea nefropatiei diabetice și promovează proliferarea MC și creșterea sintezei matricei in vitro.25 Un studiu anterior a arătat că PDGF-BB este esențial pentru proliferarea MC înainte de dezvoltare. a glomerulosclerozei în glomerulonefrita experimentală.26 După ce am confirmat că MC au fost stimulate de HG sau PDGF-BB in vitro, am detectat modificări în expresia KLF15 și SUMO1 atât la nivelul ARN cât și al proteinei.
niveluri și a constatat că aceste molecule au avut tendințe similare (Figura 2D-l). În cele din urmă, am stabilit că SUMO1 este gena țintă a KLF15.
3.4|KLF15 reglează în sus expresia genei SUMO-1 prin legarea la o regiune promotor CACCCA-SUMO-1 de 16 bp și un motiv bogat în C plus A
Am folosit suita MEME(http://meme-suite.org/tools/meme) pentru a caracteriza motivele de legare KLF15-a celor 52 de gene ecranate din datele KLF15 ChlP-Seq și am identificat motivul de legare KLF (Figura 3A). În plus, am analizat în continuare mai mult de o mie de baze în amonte de promotorul SUMO1 și am descoperit că KLF15 ar putea recunoaște și se poate lega la o secvență de 16 bp (nucleotide -205~-199), inclusiv - CACCCA-(Figura 3B).ChIP-PCR a confirmat că KLF15 este legat de promotorul SUMO1, iar rezultatele au arătat o expresie semnificativ mai mare a SUMO1 în grupul de anticorpi anti-KLF15 decât în grupul de control de fundal (Figura 3C).
În plus, am efectuat un test de raportare cu dublă luciferază pentru a confirma relația de țintire dintre SUMO1 și KLF15. Grupul de promotor SUMO1 de tip sălbatic a arătat o activitate mai mare a luciferazei decât vectorul pGL3 și grupurile mutante în HRMC, iar activitatea a fost crescută semnificativ prin supraexprimarea KLF15. Îmbunătățirile activității luciferazei au fost inversate prin transfecție cu o plasmidă care exprimă regiunea promotor mutant (Figura 3D). Luate împreună, aceste date sugerează că SUMO1 este o țintă transcripțională directă a KLF15.



3.5 |Screarea lui P53 ca substrat de SUMOilare al SUMO1
Modificările SUMO sunt modificări post-translaționale exprimate pe scară largă la eucariote. Conjugarea reversibilă a acestor modificări la proteinele substrat este cunoscută și sub numele de SUMOilare, care joacă un rol important în reglarea funcțiilor proteinelor țintă și participă în continuare la diferite procese biologice, cum ar fi transportul nucleocitoplasmatic, reglarea transcripțională, apoptoza, stabilizarea proteinelor, răspunsurile la stres și progresia ciclului celular.27 Pentru a explora moleculele de semnalizare din aval conjugate direct de SUMO1, am efectuat o analiză de rețea a SUMO1 utilizând baza de date IPA, iar datele au arătat că SUMO1 s-ar putea conjuga direct cu P53, APP, JUN și AKT, printre altele. proteine (Figura 4A-C). Am selectat inițial P53 ca o moleculă în aval a SUMO1, deoarece este o proteină bine-cunoscută care este strâns legată de proliferarea celulară.28.29 În plus, am folosit software-ul SUMOsp pentru a prezice posibilele secvențe de SUMOilare ale speciilor diferite de P53 și am constatat că P53 are secvența SUMOilare( Figura 4D). Pentru a determina dacă P53 este într-adevăr modificat prin SUMOilare, am transfectat tranzitoriu HRMC-uri cu o plasmidă de supraexpresie SUMO1 sau SUMO1 siRNA. Atât rezultatele IP, cât și cele Western blot au evidențiat tendințe ale modificărilor de expresie ale SUMO1-P53 și P53 care au fost în concordanță cu modificările. în SUMO1 (Figura 4E-J). Aceste date indică faptul că P53 este un substrat de SUMOilare al SUMO1.


3.6 |KLF15 inhibă proliferarea MC prin promovarea expresiei SUMO1 și a SUMOilării P53
Pentru a stabili reglarea SUMOilării P53 și proliferării MC de către KLF15 și SUMO1, am intervenit cu expresia KLF15 sau SUMO1 în HRMC și am tratat HRMC-urile cu PDGF-BB. Printre HRMC-urile tratate cu PDGF-BB, celulele transfectate cu plasmida de supraexpresie KLF15 au prezentat o expresie mai mare a SUMO1-P53, P53, KLF15 și SUMO1 decât celulele transfectate cu plasmida de control KLF15. Aceleași modificări în SUMO1-P53, P53 și SUMO1 au fost găsite în celulele transfectate cu plasmidă cu supraexpresie SUMO1, în timp ce expresia KLF15 a fost neschimbată în aceste celule (Figura 5A-F). PDGF-BB este unul dintre cei mai eficienți factori de creștere ai MC descriși până acum și a fost observat răspunsul proliferativ al HRMC la PDGF-BB. După cum se arată în Figura 5G, H, procentul de celule EdU-pozitive a fost crescut semnificativ prin administrarea de PDGF-BB recombinant. Rezultatele colorării EdU au indicat că atât supraexpresia KLF15, cât și SUMO1 au inhibat proliferarea celulară indusă de PDGF-BB (Figura 5G, H).

Pentru a obține mai multe informații despre rolurile KLF15 și SUMO1 în proliferarea HRMC-urilor, am transfectat celule doar cu SUMO1 siARN sau le-am cotransfectat cu SUMO1 siRNA și o plasmidă de supraexpresie KLF15. Reglarea în jos a SUMO1 nu a afectat expresia KLF15, dar nivelurile de expresie ale SUMO1-P53 și P53 au fost în mod evident scăzute după transfecția siRNA SUMO1 (Figura 6A-C). În plus, atunci când expresia SUMO1 a fost inhibată, nivelurile de expresie SUMO1-P53 și P53 au fost de asemenea suprimate chiar și în celulele care supraexprimă KLF15 (Figura 6D-F). Apoi, proliferarea MC a fost evaluată utilizând un test de colorare EdU. SUMO1 ARNi a îmbunătățit efectul proliferativ al HRMC-urilor PDGF-BBon, iar grupul cotransfectat cu plasmida de supraexpresie KLF15 și SUMO1 siRNA a avut mai multe celule EdU-pozitive decât grupul cotransfectat cu plasmida de supraexpresie și siRNA de control al secvenței hibride (Figura 6G, H) . Prin urmare, concluzionăm că KLF15 suprimă proliferarea MC prin îmbunătățirea SUMOilării P53.

3.7|Expresia globală a SUMO1 și P53 în MC glomerulare este corelată negativ cu proliferarea MC în nefrita Thy-1 la șobolan
Nefrita anti-Thy1 este un model clasic de glomerulonefrită proliferativă mezangială autolimitată cu o fază proliferativă și o fază de recuperare. Am injectat un anticorp Thy1 în șobolani Wistar pentru a crea acest model. Atât azotul ureic seric, cât și creatinina nu au nicio modificare semnificativă între șobolanii de control și șobolanii model (Figura S1). Proliferarea mezangială marcată și acumularea ECM au fost observate în timpul fazei proliferative (zilele 5 și 7) la șobolanii model, iar numărul de MC a scăzut în timpul fazei de recuperare în ziua 10 (Figura 7A). Am detectat, de asemenea, modificările de expresie în markerul de proliferare celulară PCNA prin IHC (Figura 7A, B). Nivelurile de PCNA au fost crescute în ziua 5, au atins vârful în ziua 7 și au scăzut în ziua 10 (Figura 7F). Analiza Western blot a arătat că expresia proteinei P53, SUMO1 și KLF15 în glomeruli izolați a fost mai mică în grupurile model decât în grupul martor (Figura 7C, D), în concordanță cu rezultatele imunohistochimice (Figura 7E, F). Aceste rezultate indică faptul că proliferarea anormală a MC la șobolanii model anti-Thy1 este legată de expresia la nivel scăzut a KLF15 și SUMO1. Se preconizează că interferarea cu expresia acestor molecule va atenua fenotipul patologic la șobolani.


4. DISCUTIE
Theglomerulisunt unitățile de filtrare alerinichi. Perturbarea funcției glomerulare poate fi cauzată de patologia glomerulară primară sau poate fi secundară unor boli sistemice. S-au observat modificări mezangiale în urma leziunii glomerulare, inclusiv hiperproliferarea MC, urmată de producția excesivă de ECM (expansiune mezangială) și producția de chemoatractant pentru celulele inflamatorii. Prin urmare, modularea răspunsurilor MC, în special proliferarea anormală, este o abordare terapeutică nouă. KLF15 este o proteină care joacă un rol de reglare ca factor de transcripție prin legarea de secvențe specifice de ADN. Multe studii au raportat că KLF15 este implicat în reglarea proliferării celulare. De exemplu, s-a descoperit că KLF15 participă la inhibarea căilor de semnalizare legate de proliferarea MC15,30, dar gena țintă directă nu a fost raportată în literatură. Prin urmare, acest studiu a implicat în principal screening-ul comun al nivelurilor de transcripție și translație pentru a identifica gena țintă directă a KLF15.
KLF15 reglează gene diferite în diferite specii și în diferite țesuturi și organe. În procesul de reglare a proliferării MC, KLF15 afectează expresia mai multor gene și participă la mai multe căi.131,32 Pentru a explora genele țintă directe ale KLF15, am folosit ChIP-Seg. Klein RH și colegii săi au folosit ChlP-seq tehnologie pentru a studia reglarea KLF7 asupra diferențierii celulelor epiteliale corneene.33 Ying M și colab. au folosit această tehnică pentru a studia efectul inhibitor al KLF9 asupra pluripotenței glioblastomului.34 În comparație cu cip ChlP, ChIP-Seq permite o analiză adevărată a întregului genom. cu rezoluție mai mare, sensibilitate de detecție mai mare și cerere de dimensiune mai mică a probei.35 Am folosit ChP pentru a obține fragmentele de ADN legate direct de KLF15 și, după comparare și analiză cu GenBank, am analizat 2478 de gene țintă posibile. Prin analizele GO și ale căilor, am identificat multe gene țintă implicate în ciclul celular și procesele de proliferare.
Experimentele ChlP-Seq necesită PCR pentru amplificarea semnalului de detecție și un anumit grad de părtinire în timpul procesului de amplificare este inevitabil. În plus, ChIP-Seq obține doar genele pe care KLF15 le poate lega și nu indică modificările care apar în exprimarea acestor gene atunci când expresia KLF15 se modifică. Am folosit analiza proteomică SILAC-LC/MS pentru a compensa aceste deficiențe. Această tehnică oferă informații despre toate proteinele a căror expresie se modifică la reglarea de către KLF15, inclusiv proteinele reglate direct de KLF15 și proteinele care sunt reglate indirect sau modificate post-translațional. HRMC-urile au fost cultivate folosind SILAC, iar KLF15 a fost supraexprimat în celule prin transfecția plasmidei. Proteinele au fost colectate pentru detectarea LC/MS și au fost obținute 1357 proteine exprimate diferențial. Analizele GO și ale căilor au arătat că unele dintre proteinele exprimate diferențial au fost implicate în ubiquitinare. Datele genelor și proteinelor au fost intersectate. Genele care nu au legătură cu scopul cercetării și genele neregulate direct de KLF15 au fost îndepărtate; în cele din urmă, au fost testate 52 de gene. Dintre acestea, au fost selectate cele cinci gene cu cele mai evidente diferențe de expresie care au fost cele mai strâns legate de proliferare. Având în vedere rezultatele combinate ale analizei căii, analizei exprimării SUMO1 și KLF15 în testele HRMC-uri în proliferare, ChlP-PCR și dual-luciferaze reporter, proteina SUMO1 a fost selectată ca genă țintă a KLF15.
În plus față de ubiquitină, sunt identificate un număr tot mai mare de proteine UBL,3637, inclusiv SUMO,38, 8(NEDD8)3940 cu precursor neuronal exprimat de celule, reglată în jos din punct de vedere al dezvoltării și gena 15(ISG15)41 stimulată de interferon. Aceste proteine modificatoare reglează puternic o varietate de procese biologice. Adăugarea covalentă a SUMO la substraturi, numită SUMOilare, este o modificare post-translațională implicată într-o serie de procese celulare, inclusiv transportul nuclear-citosolic, reglarea transcripțională, apoptoza, controlul stabilității proteinelor, răspunsurile la stres și progresia ciclului celular.27SUMO este de obicei atașat la resturile acceptoare de lizină ale substraturilor proteice care adăpostesc o secvență consens și contribuie la reglarea interacțiunilor proteină-proteină, precum și la compartimentarea subcelulară și stabilitatea proteinei.2 sUMO1, ca membru al familiei SUMOS, poate afecta proliferarea celulară prin modificarea substratului. și stabilizarea proteinelor de reglare a ciclului celular.43 Prin urmare, în combinație cu raportul din literatură și rezultatele cuprinzătoare ale screening-ului și analizei, ne-am concentrat asupra modului în care KLF15 reglează efectul SUMO1 asupra proliferării celulelor mezangiale.
Pentru a identifica substraturile SUMO1, am efectuat o analiză de rețea a SUMO1 utilizând baza de date IPA și software-ul SUMOsp. În combinație cu cercetările publicate asupra P53, datele noastre inițiale de screening au sugerat P53 ca o moleculă în aval a SUMO1 cu secvența SUMOylation YKxD/E. Studiile anterioare au arătat că P53 a fost un substrat al SUMOilării45, iar conjugarea îmbunătățită a P53 SUMO1 a promovat stabilitatea și activitatea lui P53 și a indus senescența.46 În studiul nostru, interferența cu expresia SUMO1 în HRMC a produs aceleași tendințe de schimbare în SUMO1-P53 și P53, indicând faptul că P53 a fost un substrat de SUMOilare al SUMO1.
Dovezile emergente au indicat că SUMOilarea și de-SUMOilarea joacă roluri în numeroase boli nefropatice, cum ar fi disgeneza renală, carcinomul renal, boala glomerulară, apoptoza podocitelor și hipertonicitatea medularei renale, leziunea renală acută și nefrolitiaza.7-51 Pentru a clarifica relația dintre KLF15, SUMO1, P53 SUMOylation și proliferarea MC, am efectuat o serie de tratamente de transfecție pe celule care au suferit proliferare indusă de PDGF-BB. Supraexprimarea KLF15 a reglat în sus expresia SUMO1, în timp ce supraexprimarea SUMO1 nu a afectat expresia KLF15. Fie supraexpresia KLF15, fie SUMO1 a crescut SUMOilarea P53 și a antagonizat proliferarea celulară indusă de PDGF-BB. Când expresia SUMO1 a fost inhibată, SUMOilarea lui P53 a fost de asemenea inhibată, iar KLF15 și-a pierdut efectul antagonist asupra proliferării celulare. In vivo. proliferarea MC a crescut treptat odată cu agravarea nefritei proliferative mezangiale, în timp ce expresia KLF15, SUMO1 și P53 a scăzut semnificativ. Având în vedere observațiile integrate în celule și țesuturi, concluzionăm preliminar că KLF15 reglează SUMOilarea P53 prin SUMO1, inhibând astfel proliferarea MC.

5. CONCLUZII
Unele studii au indicat că KLF15 joacă un rol important în reglarea proliferării MC. În această lucrare, am explorat mecanismele de suprimare a proliferării MC mediate de acest factor de transcripție. Am identificat SUMO1 ca ținta principală a KLF15 în MC prin analize bioinformatice care implică ChIP-Seq și SILAC-LC/MS. În plus, cu ajutorul bazei de date IPA și al software-ului SUMOsp, am stabilit că P53 a fost un substrat direct al SUMO1. Experimentele in vitro și in vivo au confirmat că KLF15 ar putea promova expresia SUMO1 și SUMOilarea P53, apoi inhiba proliferarea MC (Figura S2). Aceste rezultate contribuie la înțelegerea rolului de reglementare al KLF15 în proliferarea MC și oferă o bază teoretică pentru găsirea de noi tratamente pentru bolile renale legate de proliferarea MC.
