Activarea TLR9 induce glicozilarea aberantă a IgA prin căi mediate de APRIL și IL-6 în nefropatia IgA
Mar 11, 2022
A lua legatura:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Yuko Makita1 , Hitoshi Suzuki1 , Toshiki Kano1 , Akiko Takahata1 , Bruce A. Julian2,3 , Jan Novak3 și Yusuke Suzuki1
CUVINTE CHEIE: APRILIE; IgA1 cu deficit de galactoză; nefropatie IgA; IL-6; complex imun
IgA1 cu deficit de galactoză (Gd-IgA1) joacă un rol crucial în dezvoltareanefropatie IgA(IgAN). Cu toate acestea, mecanismele patogene care conduc producția de Gd-IgA1 nu au fost pe deplin elucidate. Se știe că activarea imună înnăscută prin receptorul Toll-like 9 (TLR9) este implicată în producția de Gd-IgA1. Un ligand care induce proliferarea (APRIL) și IL-6 sunt, de asemenea, cunoscute că îmbunătățesc sinteza Gd-IgA1 în IgAN. Având ca fundal, am investigat modul în care activarea TLR9 în celulele secretoare de IgA are ca rezultat supraproducția de IgA nefritogenă la șoarecele ddY predispus la IgAN și în celulele care secretă IgA1- umane. Injectarea ligandului TLR9 CpG-oligonucleotid a crescut producția de complexe imune IgA și IgG-IgA glicozilate aberant la șoarecii ddY care, la rândul lor, au exacerbatleziuni renale. Șoarecii stimulați cu oligonucleotide CpG au avut niveluri serice crescute de APRIL care s-au corelat cu cele ale complexelor imune IgA și IgG-IgA glicozilate aberant. In vitro,activare TLR9a crescut producția de IgA nefritogenă, precum și de APRIL și IL-6 în splenocitele șoarecilor ddY și în celulele secretoare de IgA1- umane. Cu toate acestea, distrugerea siRNA a lui APRIL a suprimat complet supraproducția de Gd-IgA1 indusă de IL-6. Neutralizarea IL-6 a scăzut supraproducția de Gd-IgA1 indusă de CpG-oligonucleotide. În plus, căile APRIL și IL-6, fiecare mediată independent de TLR9-indusă supraproducția de Gd-IgA1. Astfel, activarea TLR9 a îmbunătățit sinteza IgA glicozilată aberant care, într-un model de șoarece de IgAN, a îmbunătățit și mai mult leziunea renală. Prin urmare, APRIL și IL-6 în mod sinergic, precum și independent, îmbunătățesc sinteza Gd-IgA1.
Declarație translativă
Terapia specifică bolii care vizează IgA1 cu deficit de galactoză poate constitui un tratament viitor alnefropatie IgA. Rezultatele acestui studiu, care au demonstrat implicarea unui ligand care induce proliferarea (APRIL) și a interleukinei-6 (IL{-6) în supraproducția de IgA glicozilate aberant, susțin rațiunea țintirii APRIL și IL{ {3}} în nefropatia IgA (IgAN). De fapt, un studiu recent a demonstrat efectele pozitive ale anticorpului monoclonal anti-APRIL în IgAN murin1, iar un studiu clinic cu anticorp neutralizant APRIL este în curs de desfășurare la pacienții cu IgAN.
Nefropatia IgA (IgAN), cea mai frecventă glomerulonefrită primară2, cauzează boală renală în stadiu terminal la 20% până la 40% dintre pacienți în decurs de 20 de ani de la debutul acestei boli.3 Deși patogeneza IgAN rămâne pe deplin elucidată, episodic hematuria macroscopică concomitentă cu o infecție a tractului respirator superior sugerează că sistemul imunitar al mucoasei joacă un rol important în manifestările clinice ale IgAN.4

Cistanchetubulosaprevinerinichiboala, faceți clic aici pentru a obține eșantionul
Glicozilarea aberantă a IgAeste central în patogeneza IgAN. IgA glomerulară la pacienții cu IgAN este restrânsă la subclasa IgA1 și este îmbogățită pentru molecule care au niște O-glicani din regiune articulară cu deficit de galactoză (IgA1 cu deficit de galactoză [Gd-IgA1]).5,6 În plus, nivelurile serice de Gd -conținând IgA1 și IgA{11}}complexe imune(IC) cu autoanticorpi specifici Gd-IgA1 sunt crescute la pacienții cu IgAN.7–9 Cu toate acestea, mecanismele de producere a Gd-IgA1 nu sunt încă pe deplin înțelese.
Am folosit modelul de șoarece ddY predispus la IgAN în acest studiu. Șoarecii ddY dezvoltă leziuni glomerulare care le imită pe cele ale oamenilor cu IgAN.10 Deși șoarecii nu au molecule de IgA cu O-glicani tipici pentru IgA1 umană, IgAN umană și acest model de șoarece ddY predispus la IgAN au unele caracteristici specifice bolii, cum ar fi creșterea serului de IgA și IgG-IgA glicozilate aberant. IC care conțin IgA și IgA cu depunerea lor renală ulterioară și leziunea glomerulară.12 șoareci ddY prezintă proteinurie și glomerulonefrită proliferativă mezangială cu co-depunere de IgA și C3 în glomeruli. Un studiu de asociere la nivelul întregului genom a identificat loci candidați legați de progresia IgAN la șoarecii ddY.13 Locii includ gene similare din punct de vedere funcțional cu cele asociate cu IgAN uman.14,15 Aceste constatări sugerează că IgAN la șoarecii ddY și la oameni pot fi afectate. cel puțin parțial de aceleași gene de susceptibilitate. Deși caracteristicile moleculare ale IgA murină și ale IgA1 umană diferă, IgA glicozilată aberant tinde să formeze IgA polimerice și IgG-IgA IC care conduc ulterior progresia leziunii renale în modelul murin ddY al IgAN, precum și în IgAN umană. Astfel, modelul de șoareci ddY are unele caracteristici comune cu IgAN uman și poate fi un instrument util pentru analiza diferitelor caracteristici patogenetice ale IgAN.
Receptorii Toll-like (TLR) sunt molecule cheie în sistemul imunitar înnăscut și au fost implicați în patogeneza IgAN.16–20 Antigenele exogene derivate din agenți patogeni activează calea de semnalizare TLR9-MyD88.21 Acest proces duce la a crescut semnificativ sinteza de citokine inflamatorii, cum ar fi interferonul de tip 1 și interleukina-6 (IL{-6).22 Recent am demonstrat că activarea TLR9 a agravatleziuni renalela șoarecii ddY predispuși la IgAN, cu o creștere a nivelurilor serice de IgA și IgG-IgA IC.16 În plus, polimorfismele specifice TLR9 sunt asociate cu progresia bolii la pacienții cu IgAN.16 Nivelurile serice ale factorului de necroză tumorală-a și IL{{ 6}} sunt crescute la pacienții cu IgAN.23 În plus, IL-6 și IL{-4 cresc producția de IgA1 și accentuează gradul de deficit de galactoză, crescând sinteza Gd-IgA1 de către IgA{{13} }secretând linii celulare de la pacienții cu IgAN.24 Aceste constatări sugerează că IL-6 poate fi un mediator cheie al acestui proces.24,25.
Gena membrului superfamiliei 13 a ligandului factorului de necroză tumorală (TNFSF13) codifică un ligand care induce proliferarea (APRIL) care este o citokină centrală pentru maturarea și supraviețuirea celulelor B.26 APRIL împărtășește niște receptori de semnalizare importanți pentru dezvoltarea celulelor B cu altul. Ligand de superfamilie TNF, factor de activare a celulelor B (BAFF). BAFF este, de asemenea, implicat în maturarea afinității celulelor B. Un studiu de asociere la nivelul genomului a identificat TNFSF13 ca una dintre genele candidate asociate cu IgAN.27 Într-adevăr, la pacienții cu IgAN, nivelurile serice ale APRIL sunt crescute28, iar nivelurile sunt asociate cu prognosticul renal.28
Pentru a obține o mai bună înțelegere a mecanismelor de bază implicate în supraproducția de IgA glicozilate aberant prin activarea TLR9 de către ligandul CpG oligodeoxinucleotid (ODN), am folosit șoareci ddY predispuși la IgAN și celule care secretă IgA1- umane.
REZULTATE
Activarea TLR9 a agravat leziunea renală la șoarecii ddY prin producția crescută de IgA nefritogenă
TLR9 poate fi activat de liganzii corespunzători, cum ar fi CpG-ODN. Pentru a testa efectul activării TLR9 într-un model murin de IgAN, am folosit o injecție a ligandului la șoarecii ddY predispuși la IgAN. Șoarecii injectați cu CpG-ODN au dezvoltat proliferarea mezangială și expansiunea matricei extracelulare (Figura 1a). Scorurile histologice renale bazate pe proliferarea mezangială și expansiunea matricei mezangiale la șoarecii injectați cu CpG-ODN au fost semnificativ mai mari decât cele la șoarecii martor (P <{7}}.01; figura="" 1a).="" nivelurile="" de="" albumină="" urinară="" la="" șoarecii="" injectați="" cu="" cpg-odn="" au="" fost="" semnificativ="" crescute="" în="" comparație="" cu="" cele="" ale="" șoarecilor="" de="" control="" (p=""><0.{{20}}1; figura="" 1a).="" doar="" șoarecii="" injectați="" cu="" cpg-odn="" au="" dezvoltat="" depozite="" mezangiale="" de="" iga,="" igg="" și="" complement="" c3="" (figura="" 1b).="" șoarecii="" injectați="" cu="" cpg-odn="" au="" prezentat="" niveluri="" serice="" semnificativ="" mai="" mari="" de="" iga="" (p=""><0,01) și="" igg="" (p=""><0,01) decât="" șoarecii="" de="" control="" (figura="" 1c).="" iga="" serică="" de="" la="" șoareci="" injectați="" cu="" șoareci="" cpg-odn="" a="" avut="" o="" reactivitate="" mai="" mică="" cu="" ricinus="" communis="" aglutinină-i="" (rca-i)="" și="" lectinele="" de="" aglutinină="" sambucus="" nigra="" decât="" cea="" de="" la="" șoarecii="" martor="" (figura="" 1c),="" indicând="" un="" conținut="" mai="" scăzut="" de="" galactoză="" și="" acid="" sialic="" pe="" n.="" -glicanii="" iga="" murine.="" în="" plus,="" nivelul="" seric="" al="" igg-iga="" ic="" la="" șoarecii="" injectați="" cu="" cpg-odn="" a="" fost="" semnificativ="" mai="" mare="" decât="" cel="" la="" șoarecii="" de="" control="" (p=""><0,05; figura="" 1c).="" aceste="" constatări="" au="" indicat="">activare TLR9prin CpG-ODN a dus la supraproducția de IgA și IgG-IgA IC glicozilate aberant, conducând laimun-complexdepuneri și leziuni renale.
Celulele B și celulele dendritice au fost implicate în răspunsurile CpG-ODN
Am investigat ce tipuri de celule sunt implicate în inducerea supraproducției de IgA glicozilate aberant ca răspuns la CpG-ODN. Celulele B și celulele dendritice (DC) au fost izolate din splina șoarecilor ddY folosind anticorpi anti-șoarece CD19 și, respectiv, CD11c prin sortarea celulelor activate de fluorescență FL. Stimularea CpG-ODN a celulelor B izolate a indus supraproducția de IgA. În plus, CpG-ODN a crescut semnificativ producția de IgA atunci când celulele B au fost co-cultivate cu DC (Figura suplimentară S1). Aceste rezultate au sugerat că CpG-ODN a activat direct celulele B și că DCS a îmbunătățit și mai mult producția de IgA la activarea TLR9.
Supraproducția de APRIL a îmbunătățit sinteza de CI IgA și IgG-IgA glicozilate aberant
Am evaluat dacă APRIL și/sau BAFF au fost implicate în sinteza IgA nefritogenă indusă de activarea TLR9. Injectarea de CpG-ODN la șoarecii ddY a crescut semnificativ nivelurile serice ale APRIL și BAFF (Figura 2a). Nivelurile de expresie ale APRIL în splenocite s-au corelat cu producția de IgA glicozilate aberant și formarea de IgG-IgA IC (Figura 2b). Nivelurile de expresie ale BAFF în splenocite s-au corelat cu producerea de IgA glicozilate aberant, dar nu și cu formarea de IgG-IgA IC (Figura 2b). În plus, nivelurile serice ale APRIL, dar nu ale BAFF, s-au corelat semnificativ cu nivelurile serice crescute ale IgA și IgG-IgA IC glicozilate aberant la șoarecii injectați cu CpG-ODN (Figura 2c). Aceste constatări sugerează că atât APRIL, cât și BAFF pot fi implicate în producerea de IgA glicozilat aberant, deși APRIL poate fi mai implicat în producerea de IgG-IgA IC.
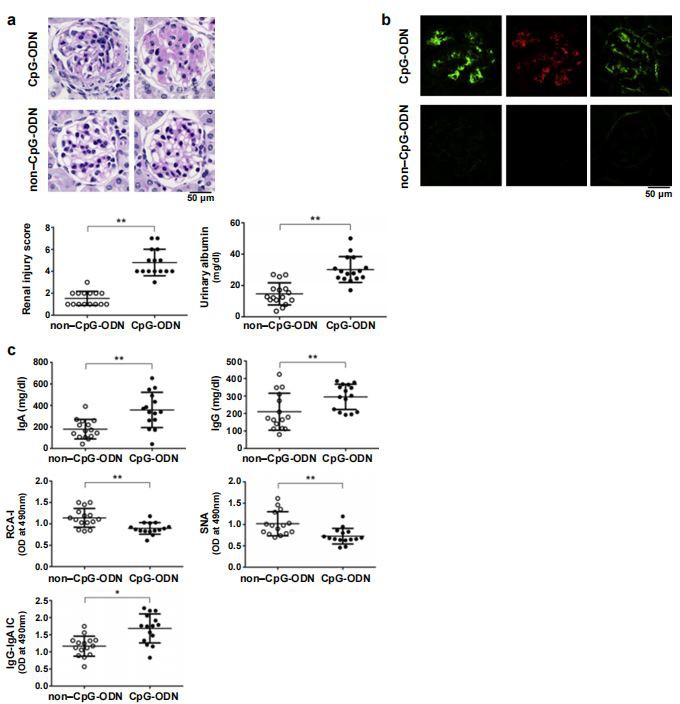
Figura 1|Producerea indusă de stimulare CpG-oligodeoxinucleotidă (ODN) de IgA nefritogenă. Injectarea cu CpG-ODN a crescut nivelurile sanguine ale complexului imun (IC) IgA și IgG-IgA glicozilat aberant și a exacerbat leziunea renală la șoarecii ddY. (a) șoareci ddY înainte de dezvoltareanefropatie IgA(IgAN) au fost injectate ip cu CpG-ODN de trei ori pe săptămână timp de 12 săptămâni. Într-o analiză histologică a leziunilor glomerulare, șoarecii injectați cu CpG-ODN au prezentat proliferarea celulelor mezangiale și expansiunea matricei extracelulare. Panoul din dreapta arată evaluarea leziunilor renale prin punctaj semicantitativ. Scorurile histologice renale, evaluate prin procente de glomeruli cu leziunile menționate mai sus, au arătat că leziunea renală la șoarecii cărora li s-a injectat CpG-ODN a fost exacerbată. Nivelurile de albumină urinară la șoarecii injectați cu CpG-ODN au fost semnificativ crescute în comparație cu cele ale șoarecilor de control. Barele din panourile inferioare ¼ înseamnă ± SEM. (b) Analiza imunohistochimică a depozitelor glomerulare de IgA, IgG și C3. Numai șoarecii injectați cu CpG-ODN au dezvoltat depozite mezangiale de IgA, IgG și C3. (c) Nivelurile serice ale IC-urilor IgA, IgG și IgG-IgA au crescut semnificativ după tratamentul cu CpG-ODN timp de 12 săptămâni. IgA serică la șoarecii injectați cu CpG-ODN a arătat o reactivitate semnificativ mai mică cu lectinele Ricinus communis aglutinină-I (RCA-I) și Sambucus nigra aglutinină (SNA) decât IgA la șoarecii martor. Aceste rezultate indică faptul că injectarea de CpG-ODN a crescut nivelurile serice ale IgA glicozilate aberant. Sunt afișate punctele individuale. *P < 0.05,="" **p="">< 0,01.="" od,="" densitate="" optică.="" pentru="" a="" optimiza="" vizualizarea="" acestei="" imagini,="" vă="" rugăm="" să="" consultați="" versiunea="" online="" a="" acestui="" articol="" la="">

Figura 2|Corelația dintre supraproducția unui ligand care induce proliferarea (APRIL) și IgA glicozilată aberant la șoarecii injectați cu CpG-oligodeoxinucleotidă (ODN). (a) Injectarea șoarecilor ddY cu CpG-ODN a crescut nivelurile serice ale factorului de activare a celulelor B (BAFF) și APRIL. (b) Nivelurile de expresie ale BAFF în splenocite întregi s-au corelat cu reactivitate redusă cu lectina Ricinus communis aglutinin-I (RCA-I), dar nu s-au corelat cu formarea complexului imun (IC) IgG-IgA. Între timp, nivelurile de expresie ale APRIL au fost asociate cu producerea de IgA glicozilate aberant și formarea de IgG-IgA IC. (c) La șoarecii injectați cu CpG-ODN, nivelurile serice de APRIL au fost asociate cu reactivitate redusă a IgA cu lectina RCA-I și niveluri crescute de IgG-IgA IC. Nivelurile serice de BAFF nu s-au corelat cu producerea de IgA glicozilate și formarea de IgG-IgA IC. Bare ¼ medie - SEM. *P < 0.05.="" od,="" densitate="">
IL-6 a indus producția de IgA glicozilate aberant
Nivelurile serice de IL{{0}} la șoarecii injectați cu CpG-ODN au fost semnificativ mai mari în comparație cu șoarecii martor (P <0,05; figura="" 3a).="" folosind="" splenocite="" ale="" șoarecilor="" ddy="" predispuși="" la="" igan,="" am="" examinat="" dacă="" activarea="" celulară="" indusă="" de="" tlr9-și="" supraproducția="" de="" iga="" glicozilate="" aberant="" au="" fost="" mediate="" de="" il-6.="" stimularea="" cpg-odn="" a="" îmbunătățit="" producția="" de="" il-6="" de="" către="" splenocite="" in="" vitro.="" adăugarea="" il-6="" în="" mediul="" de="" cultură="" al="" splenocitelor="" a="" crescut="" producția="" de="" iga.="" mai="" mult,="" il-6="" a="" îmbunătățit="" sinteza="" iga="" glicozilate="" aberant="" și="" formarea="" de="" igg-iga="" ic="" și="" a="" crescut="" producția="" de="" april="" (figura="" 3a).="" il-6-anticorp="" de="" neutralizare="" a="" redus="" iga="" totală="" indusă="" de="" cpg-odn,="" producția="" de="" iga="" glicozilate="" aberant="" și="" formarea="" de="" igg-iga="" ic="" (figura="" 3b).="" aceste="" constatări="" indică="" faptul="" că="" activarea="" tlr9="" a="" fost="" mediată,="" cel="" puțin="" parțial,="" de="" il-="" 6.="" în="" plus,="" o="" altă="" cale="" mediată="" tlr{20}}ar="" putea="" fi="" implicată="" în="" producerea="" de="" iga="" glicozilată="">

cistanchese poate îmbunătățirinichifuncţie
APRIL și IL-6 au îmbunătățit sinteza Gd-IgA1 în celulele care secretă IgA1- umane
Am testat în continuare dacă APRIL și IL-6 sunt comuni pentru mediatorii majori care sporesc producția de IgA nefritogenă în celulele secretoare de IgA1- umane. Suplimentarea CpG-ODN a îmbunătățit creșterea IL-6, expresia APRIL, producția de proteină APRIL și producția de IgA și Gd-IgA1 (Figura 4a). Stimularea cu IL-6 și cu APRIL a îmbunătățit producția de IgA și Gd-IgA1 (Figura 4b, c). Efectele stimulării CpG-ODN asupra producției de IgA și Gd-IgA1 au fost parțial reduse de anticorpii de neutralizare IL-6- (Figura 4d). Mai mult decât atât, micșorarea (si)ARN-ului APRIL de interferență a redus, de asemenea, producția de IgA și Gd-IgA1 indusă de stimularea IL-6 (Figura 4b), indicând faptul că APRIL și IL-6 promovează sinergic generarea de Gd -IgA1.
DISCUŢIE
IgA mezangială în IgAN umană este exclusivă din subclasa IgA1 care prezintă o glicozilare anormală. 29,30 IgA1 umană are o regiune balama cu O-glicani care este absentă din IgA murină.6,31,32 Cu toate acestea, glicozilarea aberantă a N-glicanilor este implicată în patogeneza unui model murin de IgAN la șoarecii ddY, cu un creșterea IgA glicozilate aberant și IC care conțin IgA.11,12 Modificările aberante ale carbohidraților IgA fie în O- sau N-glicani sunt proprietăți caracteristice ale IC care conțin IgA nefritogenă.
Mai multe studii au arătat activarea TLR9 în progresia IgAN.17–19 În studiul de față, am arătat că activarea TLR9 prin injectarea ip de CpG-ODN la șoarecii ddY a agravat leziunile renale însoțite de depozite glomerulare de IgA și IgG, probabil deoarece de niveluri serice crescute de IgA și IgG-IgA IC glicozilate aberant. Mai mult, am arătat că activarea TLR9 a fost implicată în sinteza Gd-IgA1 în liniile celulare secretoare de IgA umană.

Figura 3|Efectul CpG-oligodeoxinucleotidei (ODN) și interleukinei (IL)-6 asupra splenocitelor cultivate ale șoarecilor ddY. (a) Nivelurile serice de IL-6 la șoarecii injectați cu CpG-ODN au fost semnificativ mai mari în comparație cu șoarecii martor. Stimularea CpG-ODN a crescut producția de IL-6 a splenocitelor șoarecilor ddY în cultură. Incubarea splenocitelor șoarecilor ddY cu IL-6 recombinant a crescut producția de IgA totală și IgA glicozilată aberant, ducând la formarea complexului imun (IC) IgG-IgA. IL-6 recombinant a crescut supraproducția unui ligand care induce proliferarea (APRIL). (b) Splenocitele din cultură au fost stimulate cu CpG-ODN în prezența sau absența anticorpului de neutralizare IL-6. Anticorpul anti-IL-6 a redus producția de IgA totală și IgA glicozilată aberant și, în consecință, a redus formarea de IgG-IgA IC indusă de CpG-ODN. Bare ¼ medie ± SEM. * P < 0.05,="" **p="">< 0,01.="" od,="" densitate="" optică;="" pbs,="" soluție="" salină="" tamponată="" cu="" fosfat;="" rca-i,="" ricinus="" communis="" aglutinin-i;="" sna,="" aglutinină="" sambucus="">
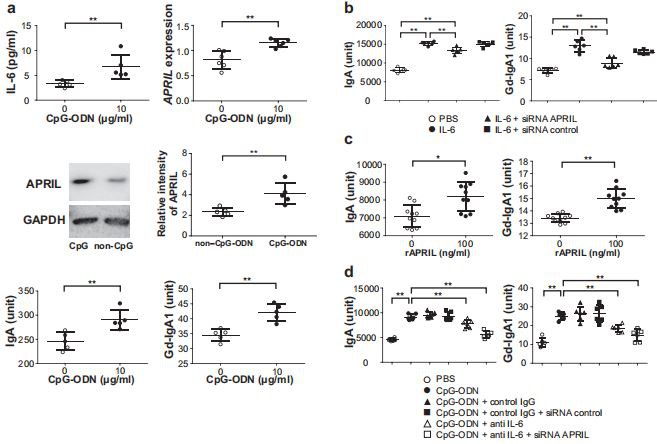
Figura 4|Efectul suplimentării CpG-oligodeoxinucleotid (ODN) sau al unui ligand care induce proliferarea (APRIL) asupra liniilor celulare secretoare de IgA1-la IgA1, IgA1 cu deficit de galactoză (Gd-IgA1) și interleukină (IL){{ 9}} producție. (a) Suplimentarea CpG-ODN a îmbunătățit producția de IL-6. CpG-ODN a îmbunătățit expresia genică a lui APRIL. Analiza Western blot a demonstrat că CpG-ODN a crescut nivelul de proteine din APRIL. Rezultatele au fost evaluate densitometric. Stimularea cu CpG-ODN a indus producerea de IgA și Gd-IgA1. (b) Reducerea ARN-ului mic, de interferență (siRNA) APRIL a redus supraproducția indusă de IL-6 de IgA și Gd-IgA1. (c) Celulele producătoare de IgA{{2{{30}}}}stimulate cu APRIL recombinant au produs mai multe IgA și Gd-IgA1. (d) Celulele care secretă IgA1-au fost incubate cu anticorp anti-IL-6 după stimularea CpG-ODN. Producția îmbunătățită de IgA și Gd-IgA1 indusă de CpG-ODN a fost redusă de anticorpul anti-IL-6 și de declanșarea siRNA a lui APRIL. Bare ¼ medie ± SEM. *P < 0,05,="" **p="">< 0,01.="" gadph,="" gliceraldehidă-3-fosfat="" dehidrogenază;="" pbs,="" soluție="" salină="" tamponată="" cu="">
Am evaluat mecanismul prin care activarea TLR9 a mediat producția îmbunătățită de IgA glicozilată aberant. BAFF și APRIL sunt cunoscute pentru rolul lor în supraviețuirea și diferențierea celulelor B. McCarthy și colab.33 au demonstrat că șoarecii transgenici care supraexprimă BAFF dezvoltă depozite de IgA mezangiale cu leziuni renale și anomalii urinare.33 Recent am demonstrat că expresia genică a APRIL este crescută în centrii germinali amigdalian ai pacienților cu IgAN. În plus, supraexprimarea APRIL în centrii germinali amigdalelor s-a corelat cu nivelurile serice de Gd-IgA1 și severitatea bolii la pacienții cu IgAN.34 Aceste constatări sugerează că atât BAFF, cât și APRIL pot fi implicate în patogeneza IgAN. Cu toate acestea, asocierea dintre activarea BAFF/APRIL și TLR9 este neclară. În studiul de față, activarea TLR9 a crescut expresia genelor și nivelurile serice ale APRIL. Nivelurile serice ale IgA glicozilate aberant au corelat cu nivelurile de expresie ale BAFF și APRIL în splenocite. Cu toate acestea, nivelurile serice ale IgG-IgA IC au corelat cu nivelurile de expresie ale lui APRIL, dar nu ale BAFF. În plus, nivelurile serice de APRIL au fost asociate cu supraproducția de IgA și IgG-IgA IC glicozilate aberant la șoarecii activați TLR9-. În celulele care secretă IgA1-, activarea TLR9 a indus, de asemenea, supraproducția de Gd-IgA1 prin APRIL. Aceste rezultate au sugerat că APRIL joacă un rol important în supraproducția indusă de TLR9-de IgA nefritogenă și formarea de IgG-IgA IC.
Răspunsul în funcție de tipul de celulă pentru a determina rolul celulelor B și T și al DC ar trebui clarificat. În studiul de față, am evaluat rolul celulelor B și al DC-urilor plasmacitoide. TLR9 este exprimat de DC, celule B și macrofage, dar nu de celulele T.35–37 Contribuția BAFF/APRIL la răspunsul anticorpului independent de celulele T este cunoscută.38,39 Aici am testat dacă activarea TLR9 poate îmbunătăți sinteza IgA glicozilată aberant și formarea de IgG-IgA IC prin APRIL într-o manieră independentă de celulele T. Am folosit, de asemenea, linii celulare secretoare de IgA1- umane clonate și am arătat că activarea TLR9 a crescut producția de Gd-IgA1 prin APRIL și IL-6, sugerând că procesul este independent de celulele T. În plus, am evaluat rolurile celulelor B și ale DC. Am arătat că CpG-ODN specific pentru celulele B și DC a crescut producția de IgA glicozilate aberant în splenocite întregi. În plus, am investigat dacă stimularea CpG-ODN in vitro poate îmbunătăți producția de IgA. Stimularea CpG-ODN a celulelor B izolate a indus supraproducția de IgA. În plus, CpG-ODN a crescut semnificativ producția de IgA atunci când celulele B au fost cocultivate cu DC (Figura suplimentară S1). Aceste rezultate sugerează că activarea CpG-ODN are ca rezultat mai mareProducția de IgA și glicozilarea aberantăeste mediată de TLR9 într-o manieră independentă de celulele T.
Se știe că IL-6 accentuează proliferarea celulelor producătoare de imunoglobuline și diferențierea terminală a celulelor plasmatice.40–42 În plus, IL-6 poate fi, de asemenea, o citokină candidată primară pentru diferențierea celulelor foliculare auxiliare T. .43,44 Celulele foliculare auxiliare T sunt esențiale pentru maturarea afinității celulelor B, recombinarea cu comutare de clasă și generarea celulelor B de memorie și a celulelor plasmatice în centrul germinal.43,44 Într-un model de șoarece cu lupus, IL-6 deficiența a prevenit diferențierea celulelor foliculare auxiliare T și expansiunea celulelor B ale centrului germinal, ducând la o producție redusă de autoanticorpi.45 Studiul prezent a clarificat faptul că activarea TLR9 de către CpG-ODN a îmbunătățit producția de IL-6 în splenocitele IgAN murine. IL-6 a indus supraproducția de IgA și IgG-IgA IC glicozilate aberant într-un model murin de IgAN. În celulele care secretă IgA1-om, am confirmat că IL-6 a îmbunătățit producția de Gd-IgA1.24 Descoperirile noastre sugerează că IL-6 poate fi una dintre moleculele majore care induc supraproducția de IgA nefritogenă. mediată de activarea TLR9.
APRIL joacă un rol important în comutarea clasei IgA și diferențierea plasmacitoidului.46,47 IL-6 promovează diferențierea terminală a celulelor B la celulele plasmatice secretoare de IgA.41,42 Studiul de față a demonstrat că IL{{7} } stimularea a indus producerea de APRILIE. Apoi am emis ipoteza că a existat o asociere între APRIL și IL-6 mediată de activarea TLR9 care a indus producția de IgA glicozilată aberant. Am constatat că anticorpul de neutralizare IL-6 nu a blocat complet supraproducția de Gd-IgA1 indusă de CpG-ODN și că eliminarea siRNA a APRIL a redus supraproducția de Gd-IgA1 indusă de IL-6. Aceste date au sugerat că APRIL și IL-6 au promovat sinergic producerea de Gd-IgA1 mediată de activarea TLR9. În plus, atât anticorpul de neutralizare IL-6, cât și declanșarea siRNA a lui APRIL au redus producția de IgA și Gd-IgA1 mai mult decât a făcut-o singur anticorpul de neutralizare IL{-6. Astfel, calea de activare a TLR9 implică efecte sinergetice IL-6 și APRIL asupra producției de anticorpi și glicozilării (Figura 5). Studii recente au indicat, de asemenea, că IL-6, în combinație cu APRIL, a indus generarea și supraviețuirea celulelor plasmatice.48,49 Cu toate acestea, sunt necesare studii viitoare pentru a clarifica căile de semnalizare intercelulară dintre APRIL și IL-6 în producerea de IgA nefritogenă.

cistanchepentrurinichiinfecţie
In concluzie,activare TLR9a exacerbat leziunea renală într-un model murin de IgAN prin creșterea producției de IgA glicozilate aberant și formarea de IgG-IgA IC. În acest proces, supraproducția de APRIL și IL-6 indusă de activarea TLR9 a sporit producția de IgA nefritogenă. În plus, studiul de față a clarificat faptul că APRIL și IL-6 funcționează sinergie, precum și independent, pentru a produce IgA glicozilată aberant. Aceste descoperiri pot informa dezvoltarea viitoare a unor noi abordări terapeutice pentru IgAN.
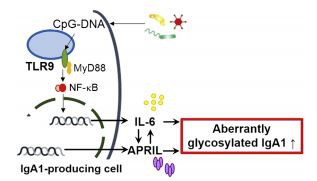
Figura 5|Rolul sinergic dintre receptorul Toll-like 9 (TLR9), un ligand care induce proliferarea (APRIL) și interleukina (IL)-6 în celulele producătoare de IgA în nefropatia IgA (IgAN). Activarea TLR9 a indus producerea de APRIL și IL-6, rezultând
supraproducția de IgA glicozilate aberant. APRIL și IL-6 funcționează sinergic pentru a promova generarea de IgA glicozilate aberant. Pe lângă faptul că APRIL induce producția de IL-6, așa cum sa raportat anterior, IL-6 poate, de asemenea, îmbunătăți sinteza lui APRIL. Mai mult, APRIL și IL-6 promovează în mod independent producerea de IgA glicozilate aberant. NF-kB, factor nuclear-kB.
METODE
Animale și protocoale experimentale
Șoarecele ddY predispus la IgAN este un model cunoscut de IgAN spontană cu incidență și amploare variabile a leziunii glomerulare care mimează IgAN uman. Șoarecii ddY 10 sunt împărțiți în 3 grupuri pe baza manifestăriiafectarea rinichilor: șoareci cu debut precoce sau tardiv și șoareci repaus. Boala cu debut precoce la șoarecii ddY prezintă proteinurie și depozite glomerulare de IgA după vârsta de 20 de săptămâni.13 Prin urmare, am folosit șoareci ddY în decurs de 18 săptămâni pentru a evalua dacă activarea TLR9 a agravat IgAN în acest model. Un total de 30 de șoareci femele ddY (SLC Japonia, Shizuoka, Japonia) au fost întreținuți la unitatea de animale a Universității Juntendo, Tokyo, Japonia. Șoarecii au fost hrăniți cu mâncare obișnuită (Oriental Yeast Co., Tokyo, Japonia) și apă ad libitum și au fost găzduiți într-o cameră specifică fără agenți patogeni. Protocolul experimental a fost aprobat de Comitetul de Etică pentru Experimentarea pe Animale al Facultății de Medicină a Universității Juntendo. La vârsta de 6 săptămâni, șoarecii au fost împărțiți aleatoriu în 2 grupuri. Un grup a primit CpG-ODN injectat ip de 3 ori pe săptămână timp de 12 săptămâni; al doilea grup (de control) a fost injectat cu non-CpG-ODN. CpG-ODN și non-CpG-ODN au fost sintetizate chimic (Invitrogen; Thermo Fisher Scientific, Kanagawa, Japonia). Secvențele ODN sunt TCGTCGTT TTCGGCGCGCGCCG sau TGCTGCTTTTGGGGGGCCCCCC (50/30) pentru CpG sau, respectiv, non-CpG ODN.
Determinarea IgA, IgG, IgG-IgA IC și a IgA glicozilate aberant în serul murin
S-au recoltat probe de sânge din vena bucală. IgA, IgG și IgG-IgA IC serice au fost măsurate prin test imunoabsorbant legat de enzime sandwich (ELISA; Bethyl Laboratories, Montgomery, TX) folosind metoda modificată bazată pe raportul nostru anterior.50 Testele de legare a lectinei au fost folosit pentru a accesa glicoforma IgA. În acest test au fost utilizate RCA-I biotinilat (Vector Laboratories, Burlingame, CA) și lectina de scoarță de Sambucus nigra (Vector Laboratories) care au recunoscut galactoza și, respectiv, acidul sialic atașați la galactoză (predominant în legătura a2,6). au fost adăugate la 100 ng de IgA per godeu. Plăcile de microtitrare acoperite cu 1 mg/ml IgA anti-șoarece de capră (100 ml/godeu) pentru cuantificarea IgA seric au fost incubate cu aceste probe și apoi a fost adăugată aglutinină Sambucus nigra sau RCA-I biotinilat. A fost aplicat conjugatul avidin-peroxidază de hrean (ExtrAvidin; Sigma-Aldrich, St. Louis, MO). Nivelurile serice ale IgA legată în mod aberant glicozilat au fost exprimate în unități (1 unitate ca densitate optică 1,0 măsurată la 490 nm). Nivelurile serice ale APRIL și BAFF au fost măsurate folosind un kit APRIL ELISA de șoarece (MyBioSource, San Diego, CA) și un kit ELISA de șoarece BAFF (R&D Systems, Minneapolis, MN), conform protocoalelor producătorului.
Test pentru Gd-IgA1 produs de celulele care secretă IgA1-umane
Un ELISA tip sandwich pentru Gd-IgA1 a fost construit folosind anticorpi specifici Gd-IgA1 (IBL, Japonia).52 Anticorpul specific Gd-IgA1 (7,5 mg/ml) diluat în soluție salină tamponată cu fosfat a fost acoperit pe o placă ELISA timp de 18 ore la temperatura camerei. Probele au fost aplicate și incubate timp de 2 ore la temperatura camerei. Plăcile au fost spălate și incubate timp de 2 ore la temperatura camerei cu un anticorp monoclonal de șoarece anti-IgA1 a1-diluat cu peroxidază de hrean diluat 1:1000- (Southern Biotech, Birmingham, AL). După spălare, plăcile au fost dezvoltate cu soluție de o-fenilendiamină SIG-MAFAST (Sigma-Aldrich), iar reacția a fost oprită prin adăugarea de acid sulfuric 1 M (Wako, Osaka, Japonia). Nivelurile de Gd-IgA1 au fost extrapolate prin referire la o curbă standard (4-ajustarea curbei logistice a parametrilor) de densitate optică la 490 nm și exprimată în unități. Gd-IgA1 generat enzimatic din plasma umană IgA152 a fost diluat în serie (1,37–1000 ng/ml) pentru a genera o curbă standard. În acest studiu, 1 unitate a fost definită ca 1 ng/mL din standardul Gd-IgA1.52
Evaluarea leziunii renale la șoarecii ddY
Rinichiwere removed after perfusion with normal saline solution. Renal tissue specimens for microscopic examination were fixed in 20% formaldehyde, embedded in paraffin, cut into 3-mm-thick sections, and then stained with periodic acid–Schiff. Specimens were quantitatively analyzed to determine the percentage of glomeruli with segmental and global sclerosis and/or mesangial cell proliferation and/or increase in the mesangial matrix. Each section was scored semiquantitatively for percentages of glomeruli with aforementioned lesions (0, 0%; 1, 1% to 24%; 2, 25% to 49%; and 3, >50 la sută din 20 de glomeruli).13,53,54 Scorul maxim total pentru fiecare secțiune a fost de 9. Probele renale pentru imunofluorescență au fost scufundate în compus cu temperatură optimă de tăiere (Sakura Finetek Japan Co., Tokyo, Japonia) și depozitate la –80 de grade. Probele au fost tăiate în secțiuni de 3-mm grosime, fixate cu acetonă la –20 de grade timp de 5 minute, spălate cu soluție salină tamponată cu fosfat, blocate cu un agent de blocare (DS Pharma Biomedical Co., Osaka, Japonia) la temperatura camerei timp de 30 de minute, și apoi incubat la temperatura camerei timp de 2 ore cu următorii anticorpi primari: IgA anti-murină de capră, IgG anti-murină de capră conjugată Alexa și anti-C3 de șobolan (Bethyl Laboratories). După încă 3 spălări cu soluție salină tamponată cu fosfat, lamelele au fost montate cu mediu de montare (Dako, Tokyo, Japonia). Probele au fost analizate și fotografiate folosind microscopie laser confocală (Olympus Corporation, Tokyo, Japonia).
Reacție cantitativă în lanț a polimerazei în timp real
ARN-ul din celulele splinei a fost extras folosind soluție de Torizol (Invitrogen, Tokyo, Japonia) și purificat cu RNeasy Mini Kit (74106; Qiagen, Valencia, CA). Reacția cantitativă în lanț a polimerazei în timp real a fost realizată utilizând sistemul de reacție în lanț a polimerazei Applied Biosystems 7500 Real-Time folosind SYBR Green PCR Master Mix (Applied Biosystems, Tokyo, Japonia) și primeri specifici: primer primer TLR9 de șoarece TCTCCCAACATGGTTCTCCGTCG, primer invers TGCAGTCCAGGCCATGA; primer MyD88 de șoarece GCACCTGTGTCTGGTCCATT, primer invers CTGTTGGA CACCTGGAGACA; și primerul direct CATTGTGGAAG GGCTCATGA, primerul invers TCTTCTGGGTGGCAGTGATG. Condițiile de amplificare au fost următoarele: preîncălzire la 95 de grade timp de 20 de secunde și apoi 40 de cicluri de denaturare la 95 de grade timp de 3 secunde și recoacere și extindere la 60 de grade timp de 30 de secunde. Testele de exprimare a genei TaqMan specifice Homo sapiens (Life Technologies, Carlsbad, CA) au fost achiziționate pentru primerul de APRIL, Hs00601664_g1, Mm{03809849-s1 și BAFF, Mm01168134-m1 . Condițiile de ciclu al reacției în lanț a polimerazei TaqMan au fost următoarele: preîncălzire la 95 de grade timp de 20 de secunde și apoi 40 de cicluri de denaturare la 95 de grade timp de 3 secunde și recoacere și extindere la 60 de grade timp de 30 de secunde
Studii in vitro cu splenocite de șoareci ddY
Splenocitele au fost cultivate în mediu Roswell Park Memorial Institute–1640 suplimentat cu 20% ser fetal de vițel, 100 mg/ml streptomicina și 100 U/ml penicilină. Globulele roșii au fost lizate în tampon de lizare a celulelor roșii din sânge (R7757; Sigma-Aldrich) la temperatura camerei timp de 1 minut, urmată de spălare în mediu Roswell Park Memorial Institute–1640. Culturile de celule au fost păstrate într-un incubator umidificat la 37 de grade cu 5 procente CO2. Clasa C CpG-ODN (TCGTCGTTTTCGGCGCGCGCCG) a fost utilizat ca ligand TLR9. IL-6 recombinant, anticorpul anti-IL{-6 și controlul izotipului IgG1 de șobolan au fost obținute de la R&D Systems. Celulele au fost cultivate cu concentrații medii sau recomandate de CpG-ODN, 10 ng/ml IL-6 recombinant și 100 ng/ml anticorp anti-IL6. IgA, IgA glicozilată aberant, IgG-IgA IC și APRIL produse de splenocite au fost măsurate prin ELISA după incubare in vitro de 72-ore.
Studii in vitro cu linii celulare1-secretoare de IgA umană
Celulele B din sângele unei persoane sănătoase au fost imortalizate cu virusul Epstein-Barr, subclonate pentru a produce linii celulare secretoare de IgA1-și cultivate conform descrierii9. În plus, am confirmat expresia receptorilor pentru APRIL/BAFF și IL. -6. Celulele au fost cultivate în mediu Roswell Park Memorial Institute–1640 suplimentat cu 20% ser fetal de vițel, streptomicina și penicilină într-un incubator umidificat la 37 de grade cu 5% CO2. Clasa B CpG-ODN (TCGTCGTTTTGTCGTTTTGTCGTT) a fost utilizat ca ligand TLR9. Anticorpul IL-6 recombinant, APRIL recombinant, anticorpul anti-IL{-6 și anticorpul de control IgG de capră au fost obținute de la R&D Systems. Celulele au fost cultivate cu concentrații medii sau recomandate de CpG-ODN, 50 ng/ml IL-6 recombinant, 40 ng/ml APRIL recombinant și 100 ng/ml anticorp anti-IL{-6 timp de 72 de ore
Western blot
Supernatanții din celulele secretoare de IgA1-au fost separați prin electroforeză pe gel de dodecil sulfat de sodiu-poliacrilamidă în condiții reducătoare folosind geluri cu gradient de 5 până la 15%. Gelurile au fost transferate pe membrane de difluorură de poliviniliden și incubate cu anticorpi specifici pentru APRIL (Abcam Inc., Cambridge, MA) și gliceraldehida-3-fosfat dehidrogenază (Abcam Inc). Petele au fost vizualizate prin chemiluminiscență folosind chemiluminiscență îmbunătățită (GE Healthcare, Tokyo, Japonia) și detector de luminiscență (Konica Minolta Healthcare, Tokyo, Japonia). Rezultatele au fost evaluate densitometric.
APRILIE doborârea siRNA
Celulele care secretă IgA1-umane au fost cultivate în plăci de cultură de 24-godeuri și transfectate cu siARN specific APRIL (GS8741, Qiagen) sau control nețintire siRNA (GS10673, Qiagen) folosind protocolul de transfecție conform instrucțiunilor producătorului . După incubare timp de 24 de ore, celulele au fost incubate cu 50 ng/ml IL-6 recombinant (R&D Systems) timp de 72 de ore. După incubare, celulele și supernatanții au fost recoltați pentru măsurarea IgA și Gd-IgA1.
analize statistice
Corelația dintre diferiți parametri a fost analizată folosind o analiză a varianței. Datele au fost exprimate ca medie ± SD sau valori mediane. Valorile p < {{0}},05="" au="" fost="" considerate="" semnificative="" statistic.="" toate="" analizele="" statistice="" au="" fost="" efectuate="" folosind="" graphpad="" prism="" versiunea="" 6.0="" pentru="" windows="" (graphpad="" software,="" san="" diego,="">

cistanchepentrurinichisimptomele bolii
DEZVĂLUIRE
Toți autorii au declarat că nu există interese concurente.
MULȚUMIRI
Acest studiu a fost susținut parțial de JSPS KAKENHI Grant No. 18K08252 și Proiectul de cercetare practică pentru boli renale de la Agenția Japoneză pentru Cercetare și Dezvoltare Medicală, AMED. JN și BAJ au fost susținute parțial de subvențiile National Institutes of Health DK078244 și DK082753. Mulțumim doamnei Terumi Shibata pentru asistența tehnică excelentă. De asemenea, mulțumim doamnei Takako Ikegami și doamnei Tomomi Ikeda (Divizia de Cercetare Moleculară și Biochimică, Școala de Medicină a Universității Juntendo) și doamnei Tamami Sakanishi (Divizia de Biologie Celulară, Școala de Medicină a Universității Juntendo) pentru asistența tehnică excelentă. .
MATERIAL SUPLIMENTAR
Fișier suplimentar (PDF)
Figura S1. Celulele B activate de CpG-oligodeoxinucleotide (ODN) și celulele dendritice (DC) îmbunătățesc și mai mult producția de IgA. Celulele B și DC au fost izolate din splina șoarecilor ddY. Stimularea CpG-ODN a crescut producția de IgA în celulele B izolate. Această creștere a fost îmbunătățită în continuare prin co-cultivarea celulelor B cu DC. *P < 0.05.="" metodele="" detaliate="" sunt="" furnizate="" în="" metodele="" suplimentare.="" metode="">
REFERINȚE
1. Myette JR, Kano T, Suzuki H, et al. Un anticorp țintit cu ligand care induce proliferarea (APRIL) este un tratament sigur și eficient al nefropatiei murine cu IgA. Rinichi Int. 2019;96:104–116.
2. Levy M, Berger J. Perspectiva mondială a nefropatiei IgA. Am J Rinichi Dis. 1988;12:340–347.
3. D'Amico G. Cea mai frecventă glomerulonefrită din lume: nefropatia IgA. QJ Med. 1987;64:709–727.
4. Feehally J, Beattie TJ, Brenchley PE, et al. Studiu secvenţial al sistemului IgA în nefropatia IgA recidivante. Rinichi Int. 1986;30:924–931.
5. Wyatt RJ, Julian BA. nefropatie IgA. N Engl J Med. 2013;368:2402–2414.
6. Suzuki H, Yasutake J, Makita Y, et al. Nefropatia IgA și vasculita IgA cu nefrită au o caracteristică comună care implică patogenia orientată IgA1- cu deficit de galactoză. Rinichi Int. 2018;93:700–705.
7. Glassock RJ. Analiza activității anticorpilor în nefropatia IgA. J Clin Invest. 2009;119:1450–1452.
8. Moldoveanu Z, Wyatt RJ, Lee JY, et al. Pacienții cu nefropatie IgA au niveluri serice de IgA1 cu deficit de galactoză crescute. Rinichi Int. 2007;71: 1148–1154.
9. Suzuki H, Moldoveanu Z, Hall S, et al. Liniile celulare care secretă IgA1-de la pacienții cu nefropatie IgA produc IgA1 glicozilat aberant. J Clin Invest. 2008;118:629–639.
10. Imai H, Nakamoto Y, Asakura K, et al. Depunerea spontană de IgA glomerulară la șoarecii ddY: un model animal de nefrită IgA. Rinichi Int. 1985;27:756–761.
11. Okazaki K, Suzuki Y, Otsuji M, et al. Dezvoltarea unui model de nefropatie IgA cu debut precoce. J Am Soc Nephrol. 2012;23:1364–1374.
12. Nishie T, Miyaishi O, Azuma H, et al. Dezvoltarea unei boli asemănătoare nefropatiei imunoglobulinei A la șoarecii cu deficit de beta-1,4-galactosiltransferază-I. Sunt J Pathol. 2007;170:447–456.
13. Suzuki H, Suzuki Y, Yamanaka T, et al. Scanarea la nivel de genom într-un model nou de nefropatie IgA identifică un locus de susceptibilitate pe cromozomul murin 10, într-o regiune sintetică cu IGAN1 uman de pe cromozomul 6q22-23. J Am Soc Nephrol. 2005;16:1289–1299.
14. Takei T, Iida A, Nitta K, et al. Asocierea dintre polimorfismele cu o singură nucleotidă în genele selectinei și nefropatia imunoglobulinei A. Am J Hum Genet. 2002;70:781–786.
15. Gharavi AG, Yan Y, Scolari F, et al. Nefropatia IgA, cea mai frecventă cauză a glomerulonefritei, este legată de 6q22-23. Nat Genet. 2000;26:354–357.
16. Suzuki H, Suzuki Y, Narita I, et al. Receptorul toll-like 9 afectează severitatea nefropatiei IgA. J Am Soc Nephrol. 2008;19:2384–2395.
17. Nakata J, Suzuki Y, Suzuki H, et al. Modificări ale IgA1 cu deficit de galactoză seric nefritogenă în nefropatia IgA după amigdalectomiei și terapiei cu steroizi. Plus unu. 2014;9:e89707.
18. Sato D, Suzuki Y, Kano T, et al. Expresia TLR9 amigdaliană și eficacitatea amigdalectomiei cu terapia cu puls steroizi la pacienții cu nefropatie IgA. Transplant Nephrol Dial. 2012;27:1090–1097.
19. Coppo R, Camilla R, Amore A, et al. Expresiile receptorului Toll-like 4 sunt crescute în celulele mononucleare circulante ale pacienților cu nefropatie cu imunoglobulină A. Clin Exp Immunol. 2010;159:73–81.
20. Maiguma M, Suzuki Y, Suzuki H, et al. Zincul alimentar este un modificator cheie de mediu în progresia nefropatiei IgA. Plus unu. 2014;9: e90558.
21. Kawai T, Akira S. Semnalizarea la NF-kappaB de către receptorii Toll-like. Trends Mol Med. 2007;13:460–469.
22. Kuwata H, Matsumoto M, Atarashi K, et al. IkappaBNS inhibă inducerea unui subset de gene dependente de receptorul Toll-like și limitează inflamația. Imunitate. 2006;24:41–51.
23. Rostoker G, Rymer JC, Barnard G, et al. Dezechilibre în citokinele proinflamatorii serice și receptorii lor solubili: un rol presupus în progresia nefropatiei IgA idiopatice (IgAN) și a nefritei purpurei Henoch Schönlein și o țintă potențială a terapiei cu imunoglobuline? Clin Exp Immunol. 1998;114:468–476.
24. Suzuki H, Raska M, Yamada K, et al. Citokinele modifică O-glicozilarea IgA1 prin dereglarea enzimelor C1GalT1 și ST6GalNAc-II. J Biol Chem. 2014;289:5330–5339.
25. Yamada K, Huang ZQ, Raska M, et al. Inhibarea semnalizării STAT3 reduce producția de autoantigen IgA1 în nefropatia IgA. Kidney Int Rep. 2017;2:1194–1207.
26. Schneider P, MacKay F, Steiner V, et al. BAFF, un nou ligand din familia factorului de necroză tumorală, stimulează creșterea celulelor B. J Exp Med. 1999;189: 1747–1756.
27. Kiryluk K, Li Y, Scolari F, et al. Descoperirea de noi loci de risc pentru nefropatia IgA implică gene implicate în imunitate împotriva agenților patogeni intestinali. Nat Genet. 2014;46:1187–1196.
28. Han SS, Yang SH, Choi M, et al. Rolul membrului 13 al superfamiliei TNF în progresia nefropatiei IgA. J Am Soc Nephrol. 2016;27:3430– 3439.
29. Hiki Y, Odani H, Takahashi M, et al. Spectrometria de masă dovedește glicozilarea sub-O a IgA1 glomerulară în nefropatia IgA. Rinichi Int. 2001;59: 1077–1085.
30. Allen AC, Bailey EM, Brenchley PE, et al. IgA1 mezangială în nefropatia IgA prezintă O-glicozilare aberantă: observații la trei pacienți. Rinichi Int. 2001;60:969–973.
31. Hiki Y. Oligozaharide O-legate din regiunea balama IgA1: rolurile structurii sale aberante în apariția și/sau progresia nefropatiei IgA. Clin Exp Nephrol. 2009;13:415–423.
32. Mestecky J, Tomana M, Moldoveanu Z, et al. Rolul glicozilării aberante a moleculelor IgA1 în patogeneza nefropatiei IgA. Presă de sânge pentru rinichi Res. 2008;31:29–37.
33. McCarthy DD, Kujawa J, Wilson C, et al. Șoarecii care supraexprimă BAFF dezvoltă o nefropatie asociată cu IgA, dependentă de flflora comensală. J Clin Invest. 2011;121:3991–4002.
34. Muto M, Manfroi B, Suzuki H, et al. Stimularea receptorului 9 asemănător Toll induce expresia aberantă a unui ligand care induce proliferarea de către celulele B ale centrului germinal amigdalian în nefropatia IgA. J Am Soc Nephrol. 2017;28:1227–1238.
35. Latz E, Schoenemeyer A, Visintin A, et al. TLR9 semnalează după translocarea de la ER la ADN-ul CpG în lizozom. Nat Immunol. 2004;5:190–198.
36. Hornung V, Rothenfusser S, Britsch S, et al. Expresia cantitativă a mARN-ului receptorului de tip toll 1-10 în subseturi celulare de celule mononucleare din sângele periferic uman și sensibilitate la oligodeoxinucleotidele CpG. J Immunol. 2002;168:4531–4537.
37. Kadowaki N, Ho S, Antonenko S, et al. Subseturi de precursori de celule dendritice umane exprimă diferiți receptori de tip toll și răspund la diferiți antigeni microbieni. J Exp Med. 2001;194:863–869.
38. He B, Xu W, Santini PA, et al. Bacteriile intestinale declanșează schimbarea clasei imunoglobulinei A(2) independente de celulele T prin inducerea secreției de celule epiteliale a citokinei APRIL. Imunitate. 2007;26:812–826.
39. Mackay F, Schneider P. Schimbarea codului BAFF. Nat Rev Immunol. 2009;9: 491–502.
40. Kunimoto DY, Nordan RP, Strober W. IL-6 este un cofactor puternic al IL-1 în sinteza IgM și al IL-5 în sinteza IgA. J Immunol. 1989;143:2230–2235.
41. Beagley KW, Eldridge JH, Lee F, et al. Interleukine și sinteza IgA. Interleukina 6 umană și murină induc secreția de IgA cu viteză ridicată în celulele B angajate de IgA. J Exp Med. 1989;169:2133–2148.
42. Ramsay AJ, Husband AJ, Ramshaw IA, et al. Rolul interleukinei-6 în răspunsurile anticorpilor IgA mucoase in vivo. Ştiinţă. 1994;264:561–563.
43. Nurieva RI, Chung Y, Martinez GJ, et al. Bcl6 mediază dezvoltarea celulelor T helper foliculare. Ştiinţă. 2009;325:1001–1005.
44. Poholek AC, Hansen K, Hernandez SG, et al. Reglarea in vivo a dezvoltării celulelor helper foliculare Bcl6 și T. J Immunol. 2010;185: 313–326.
45. Jain S, Park G, Sproule TJ, et al. Interleukina 6 accelerează mortalitatea prin promovarea progresiei bolii asemănătoare lupusului eritematos sistemic a șoarecilor BXSB.Yaa. Plus unu. 2016;11:e0153059.
46. Litinskiy MB, Nardelli B, Hilbert DM, et al. DC induc schimbarea clasei de imunoglobuline independente CD40-prin BLyS și APRIL. Nat Immunol. 2002;3:822–829.
47. Castigli E, Wilson SA, Scott S, et al. TACI și BAFF-R mediază schimbarea izotipului în celulele B. J Exp Med. 2005;201:35–39.
48. Jourdan M, Chen M, Robert N, et al. IL-6 sprijină generarea de celule plasmatice umane cu viață lungă în combinație cu factori APRIL sau cu factori solubili în celulele stromale. leucemie. 2014;28:1647–1656.
49. Chu VT, Fröhlich A, Steinhauser G și colab. Eozinofilele sunt necesare pentru menținerea celulelor plasmatice în măduva osoasă. Nat Immunol. 2011;12: 151–159.
50. Suzuki H, Suzuki Y, Aizawa M, et al. Polarizarea Th1 în nefropatia murină IgA dirijată de celulele derivate din măduva osoasă. Rinichi Int. 2007;72: 319–327.
51. Chintalacharuvu SR, Emancipator SN. Glicozilarea IgA produsă de celulele B murine este alterată de citokinele Th2. J Immunol. 1997;159:2327–2333.
52. Yasutake J, Suzuki Y, Suzuki H, et al. Nouă abordare independentă de lectină pentru a detecta IgA1 cu deficit de galactoză în nefropatia IgA. Transplant Nephrol Dial. 2015;30:1315–1321.
53. Katafuchi R, Kiyoshi Y, Oh Y, et al. Scorul glomerular ca prognosticator în nefropatia IgA: utilitatea și limitarea acestuia. Clin Nephrol. 1998;49:1–8.
54. Ballardie FW, Roberts IS. Studiu prospectiv controlat de prednisolon și citotoxice în nefropatia progresivă cu IgA. J Am Soc Nephrol. 2002;13: 142–148.






