Mecanismul de protecție a rinichilor al Cistanche: activarea receptorului de hidrocarburi arii mediază boala renală și carcinomul cu celule renale
Mar 13, 2022
Activarea receptorului de hidrocarburi arii mediază boala renală și carcinomul cu celule renale
A lua legatura:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Abstract
Thereceptor de hidrocarburi arii(AhR) este un bine-cunoscut factor de transcripție citoplasmatic activat de ligand care contribuie la răspunsurile celulare împotriva toxinelor din mediu și a agenților cancerigeni. AhR este activat de o serie de compuși structural diverși din mediu, microbiom, produse naturale și metabolismul gazdei, ceea ce sugerează că AhR posedă un situs de legare a liganzilor destul de promiscuu. Studiile în creștere au indicat că AhR poate fi activat de o varietate de liganzi endogeni și poate induce expresia unei baterii de gene AhR reglează o varietate de evenimente fiziopatologice, inclusiv proliferarea celulară, diferențierea, apoptoza, adeziunea și migrarea. Aceste noi roluri ne-au extins înțelegerea căilor de semnalizare AhR și a interacțiunii metaboliților endogeni cu AhR în condiții homeostatice și patologice. Studii recente au demonstrat că AhR este legat de bolile cardiovasculare (CVD),boală cronică de rinichi,și carcinom cu celule renale (RCC). În această revizuire, rezumăm liganzii derivați din microbiota intestinală care induc activitatea AhR la pacienții cuboală cronică de rinichi. BCV, nefropatia diabetică și RCC pot oferi o nouă abordare diagnostică și prognostică pentru afectarea renală complexă. Evidențiem în continuare polifenolii din produse naturale, cum ar fi AhRagoniştii sau antagoniştii care reglează activitatea. O mai bună înțelegere a polifenolilor diverși structural și a activităților biologice AhR ne-ar permite să le lămurim mecanismul molecular și să descoperim potențiale strategii terapeutice care vizează activarea AhR.Cistancheeste o planta tonica binecunoscuta care poate hrani si proteja rinichii. În teoria medicinei tradiționale chineze,Cistancheeste cea mai bună plantă pentru rinichi.Cistancheeste bogat în echinacozide, acteozide și flavonoide. Aceste ingrediente eficiente înCistanchepoate reduce apoptoza celulelor renale și poate crește proliferarea celulelor renale. Prin urmare,Cistancheeste un supliment natural pentru rinichi.
Cuvinte cheie:Receptor de hidrocarburi arii, Boala cronică de rinichi, Microbiota intestinală, Toxine uremice, Carcinom renal, Produse naturale, Cistanche
Hui Zhao, Lin Chen, Tian Yang, Ya‑Long Feng, Nosratola D. Vaziri, Bao‑Li Liu, Qing‑Quan Liu, Yan Guo și Ying‑Yong Zhao

rinichirănireiar boala poate fi prevenită princistanche
fundal
Inducerea unei baterii de gene care codifică enzime care metabolizează xenobioticele ca răspuns la deteriorarea chimică este un răspuns adaptativ în multe organisme. Thereceptor de hidrocarburi arii(AhR) este un mediator al răspunsului toxic al poluanților ubicui de mediu, cum ar fi hidrocarburile aromatice halogenate, hidrocarburile aromatice policiclice și bifenilii policlorurați coplanari [1–3], inclusiv 2,3,7,8-tetraclorodibenzo-p- dioxina (TCDD), care are efecte cancerigene și teratogene [4]. AhR este descris ca o perioadă de senzor de mediu-receptor de hidrocarburi ariiProteina translocator nuclear-unic (Per-ARNT-Sim) care aparține unui membru al familiei factorilor de transcripție de bază helix-loop-helix [5].
Semnalizarea AhR și liganzii săi
semnalizare AhR
AhR este un factor de transcripție mediat de liganzi implicat în detoxifierea biologică a liganzilor [6]. După cum se arată în Fig. 1, în condiții bazale, AhR este localizat în citoplasmă într-o stare inactivă, ca parte a unui complex format cu proteine stabilizatoare, inclusiv 2 molecule de proteină de șoc termic 90 (HSP90), o moleculă de cochaperone p23 (P23). ) și o moleculă de proteină 2 asociată cu X (XAP2) [1]. Când un ligand se leagă de AhR, complexul AhR/ligand/Hsp90/XAP2 se translocă în nucleu și se dimerizează cu translocatorul nuclear AhR (ARNT). AhR este activat de o alterare conformațională care își expune secvența de localizare nucleară. După ce AhR este fosforilat de protein kinaza C, complexul AhR este translocat în nucleu [7]. În nucleu, complexul eliberează proteina, astfel încât să se poată lega de ARNT prin domeniul său Per-ARNT-Sim, conducând la dimerul AhR-ARNT. Acest heterodimer AhR/ARNT este recunoscut de un situs specific ADN-ului, 5′-GCGTG-3′, secvența DRE sau XRE (element sensibil la dioxină sau xenobiotic) situată în promotorii genelor țintă și declanșează acestea. transcriere, cum ar fi citocromul P450, familia 1, membrul 1A (CYP1A1); citocromul P450, familia 1, membru 2A (CYP1A2); citocromul P450, familia 1, subfamilia B (CYP1B1); represor AhR (AhRR); și ciclooxigenază-2 (COX-2). AhR induce expresia enzimelor xenobiotice, cum ar fi genele citocromului P450, necesare pentru detoxicarea liganzilor toxici AhR [1].

Activarea AhR este recunoscută în primul rând pentru a media expresia genelor de metabolizare a medicamentelor de fază I și II, inclusiv CYP1A1, CYP1A2, CYP1B1, UGT1A1/6 și sulfotransferaza (SULT)1A1. Studiile de creștere au demonstrat că calea AhR este asociată cu diverse funcții fiziologice și procese de boală, cum ar fi reglarea diferențierii celulelor T și dezvoltarea embrionară/fetală, medierea stresului oxidativ și răspunsurile inflamatorii [8-13]. Semnalizarea AhR tradițională nu poate explica toate funcțiile celulare atribuite AhR. În plus față de calea canonică de reglare a genelor, a fost descrisă semnalizarea AhR necanonică care include diafonia cu alți factori de transcripție, inclusiv factorul nuclear kappa B (NF-κB), factorul 2 asociat factorului nuclear eritroid-2-(Nrf2), moartea programată-ligand 1 și proteina activatoare 1 (în special subunitatea RelA), proteina retinoblastomului hipofosforilat, receptorul de estrogen corepresor și receptorul de progesteron [14–16] (Fig. 1 și 2). În plus, AhR citosolic poate activa o multitudine de alte proteine citosolice, inclusiv -catenina, Smads, familia p38 de protein kinaza activată de mitogen (MAPK), kinaza reglată de semnal extracelular (ERK) și kinaza terminală Jun-NH2- (JNK) [17] (Fig. 2).
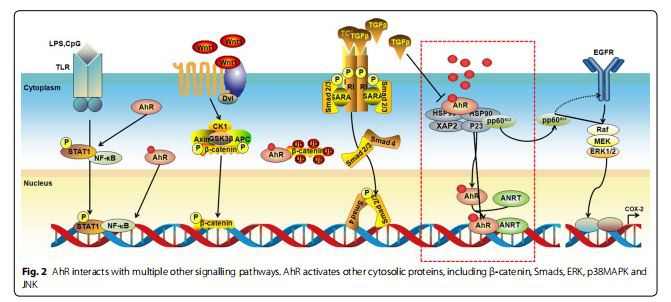
Liganzi ai semnalizării AhR activate
Există dovezi în curs de dezvoltare că expunerea cronică la substanțele chimice din mediu prin aer și dietă, în special poluanții organici persistenti, cum ar fi TCDD sau dioxina, provoacă efecte secundare prin inducerea activată de ligand a căii AhR [18-20] (Fig. 1). Mai mult, există, de asemenea, o multitudine de candidați liganzi AhR endogeni, cum ar fi eicosanoizii (de exemplu, lipoxina A4, bilirubină și lipopolizaharide) și o multitudine de flavonoide care apar în mod natural (de exemplu, resveratrol și quercetină). Acești metaboliți endogeni au fost identificați ca liganzi AhR slabi datorită afinității lor scăzute pentru AhR (de exemplu, bilirubină și indirubină). Cu toate acestea, bilirubina poate activa AhR la o anumită concentrație în anumite stări de boală, cum ar fi icterul [21]. AhR uman se leagă de indirubină de preferință în comparație cu AhR de șoarece [22].
Activarea AhR prin toxine uremice cu greutate moleculară mică Metabonomica, care a fost definită ca „măsurarea cantitativă a răspunsului metabolic dinamic multiparametric al organismelor vii la stimularea fiziopatologică sau modificările genetice” [23, 24], este folosită ca o metodă cuprinzătoare de a se adresează modificărilor metaboliților cu greutate moleculară mică (MW<1000 da)="" following="" disease,="" toxic="" exposure="" or="" variation="" in="" genetic="" function="" [25–28].="" mounting="" studies="" by="" using="" burgeoning="" metabonomics="" have="" demonstrated="" that="" low-molecular-weight="" metabolites,="" such="" as="" cholesterols,="" amino="" acids,="" vitamins,="" lipids,="" carbohydrates,="" minerals,="" and="" other="" compounds,="" play="" a="" critical="" role="" in="" health="" and="" diseases="" [29–33].="" several="" novels="" or="" known="" metabolites="" have="" been="" used="" for="" disease="" diagnosis="" and="" prognosis,="" new="" drug="" discovery,="" and="" toxicity="" evaluation="">
Scăderea funcției renale duce la reținerea diverșilor metaboliți [41–45] care sunt reținuți în sânge și diferite țesuturi în loc să fie excretați de rinichi [46]. Astfel, reținerea acestor metaboliți contribuie la o varietate de boli, în specialboală cronică de rinichiși boli cardiovasculare (BCV) [47–50].Boala cronică de rinichiduce la reținerea unuia dintre cei mai importanți metaboliți, așa-numiții soluți uremici. În 2003, Grupul de lucru european privind toxinele uremice a clasificat 90 de compuși uremici [51]. Numărul de compuși/metaboliți a fost extins de atunci [51]. Toxinele uremice sunt clasificate clasic în funcție de caracteristicile fizico-chimice care afectează eliminarea lor prin dializă: molecule scăzute solubile în apă (MW).<500 da),="" larger="" middle="" molecules="" (mw="">500 Da) și molecule legate de proteine [52]. Soluțiile uremice legate de proteine sunt slab îndepărtate prin dializă convențională. Dintre toxinele uremice, toxinele uremice derivate din triptofan prezintă un interes deosebit, deoarece sunt implicate în toxicitatea cardiovasculară și s-au dovedit a fi liganzi AhR puternici [53, 54]. Triptofanul este un aminoacid esențial care se găsește în dietă. După cum se arată în Fig. 3, 95% triptofan poate fi metabolizat prin calea chinureninei, care este mediată de enzimele limitatoare ale vitezei triptofan 2,3-dioxigenază (TDO) și indoleamină 2,3-dioxigenază ( IDO) [55]. TDO este foarte exprimat în ficat. IDO are două izoenzime, IDO1 și IDO2. Expresia IDO1 a fost demonstrată în majoritatea țesuturilor [55]. Activitatea IDO care duce de la triptofan la chinurenină este reflectată de raportul triptofan/chinurenină [56]. Triptofanul seric este scăzut înboală cronică de rinichipacienți, în timp ce metaboliții din calea chinureninei, inclusiv chinurenina, acidul chinurenin, 3-hidroxichinurenina, acidul antranilic și acidul chinolinic, sunt crescuti. Alte două căi metabolice ale triptofanului sunt calea serotoninei, care produce melatonină, și calea metabolică indolice, care produce compuși indolici, inclusiv indoxil sulfat (IS), acid indol-3-acetic (IAA) și indoxil{{2} }d glucuronid (IDG) (Fig. 3). În calea indolică, triptofanul este convertit în indol prin microbiota intestinală și absorbit în circulația sanguină [57] (Fig. 3). De exemplu, triptofanaza produsă din Escherichia coli metabolizează triptofanul alimentar în indol și derivații săi [58]. În ficat, indolul derivat din bacterii este metabolizat în continuare la IS prin SULT1A1 uman [59]. Mai mult, indolul este oxidat la IS de către CYP2E1 microzomal [60]. IAA este produs direct în intestin prin metabolismul triptofanului sau endogen în țesut prin triptamină [60]. De exemplu, triptofan mono-oxigenaza produsă de Arthrobacter trece și triptofan decarboxilaza produsă de Clostridium sporogenes convertesc triptofanul în liganzii AhR IAA și, respectiv, triptamină [61–63]. Într-o stare sănătoasă, microbiota intestinală umană desfășoară mai multe activități pentru organism. Microbiota intestinală trăiește într-o relație comensală cu gazda, protejând împotriva agenților patogeni, modulând sistemul imunitar și reglând metabolismul endogen al lipidelor și carbohidraților, menținând astfel echilibrul nutrițional [64]. Un număr tot mai mare de studii recente au demonstrat că modificările microbiotei intestinale sunt legate de o multitudine de boli, cum ar fi cancerul, obezitatea, diabetul, bolile cardiovasculare, bolile inflamatorii intestinale și bolile de rinichi [65]. Este din ce în ce mai recunoscut că metabolismul microbiotei intestinale contribuie la generarea de toxine uremice enorme [66–69].
Deși toxinele uremice contribuie la diferite boli asociate cu o varietate de mecanisme de acțiune, unii metaboliți, cum ar fi metaboliții de hidrocarburi aromatice și derivații de indol, s-au dovedit ca liganzi endogeni AhR și astfel ar putea evoca activarea AhR [70]. Studii ulterioare au indicat că AhR pare să simtă insultele microbiene și factorii de virulență bacteriană, constituind un nou ligand AhR [71]. Dovezile tot mai mari au demonstrat, de asemenea, că toxinele uremice derivate din metabolismul triptofanului, cum ar fi IS, IAA și IDG, sunt recunoscuți ca cei mai importanți liganzi endogeni AhR și astfel pot declanșa activarea AhR [72, 73] (Fig. 3). IS, IAA și IDG pot activa semnalizarea AhR prin legarea directă la complexul AhR/Hsp90/XAP2. Atât IS, cât și IAA reglează în sus opt gene ale AhR, inclusiv CYP1A1 și CYP1B1 [74].
IS a fost raportat ca una dintre cele mai importante toxine uremice. A fost examinat un panou de derivați de indol, inclusiv triptofan, indol, IS, IAA și indol 3-metanol ca liganzi AhR [59]. IS a fost demonstrat ca un ligand endogen puternic care activează selectiv AhR uman la un nivel nanomolar în hepatocitele umane primare, mediand transcrierea mai multor gene AhR, inclusiv CYP1A1, CYP1A2, CYP1B1, UGT1A1, UGT1A6, interleukina 6 și amiloid A11 seric. În plus, IS exercită o potență de 500- ori mai mare în activarea transcripțională a AhR umană în comparație cu AhR de șoarece [59]. Descoperirile structurii-funcție au indicat că gruparea sulfat este un factor important pentru activarea eficientă a AhR. Analizele de legare a competiției ligandului au indicat că IS este un ligand AhR direct [59]. Studiile anterioare au arătat că IS suprimă proliferarea endotelială, inhibă repararea rănilor și declanșează stresul oxidativ [72]. IS a fost implicat în mortalitatea cardiovasculară și în factorii de risc clasici înBoala cronică de rinichipacientii. Nivelurile bazale de AhR reglează funcția podocitelor în circumstanțe normale, iar suprareglarea activării AhR în podocite de către IS contribuie la leziunea glomerulară [75]. AhR activat de IS declanșează un fenotip proinflamator, leziuni podocice și leziuni glomerulare atât in vivo, cât și in vitro [75]. Un alt studiu a raportat că creșterea IS a afectat metabolismul fierului în indusă de adeninăBoala cronică de rinichișoarecii prin participarea la reglarea hepcidinei prin AhR și căile de stres oxidativ [76]. Mai mult, activarea AhR a mediat expresia suprareglată mediată de IS a proteinei chemoatractante monocite -1 (MCP-1) în celulele endoteliale ale venei ombilicale umane (HUVEC) [77]. IAA este o altă toxină uremică importantă. IAA activează calea de semnalizare AhR/p38MAPK/NF-κB, care induce expresia COX-2, iar IAA crește producția de specii reactive de oxigen atât in vivo, cât și in vitro [78]. Prin urmare, IS sau IAA seric ar putea fi un indicator independent al evenimentelor cardiovasculare și al mortalității înboală cronică de rinichipacientii.
Alte toxine din metabolismul triptofanului raportate ca liganzi AhR provin din calea chinureninei. Acidul kinurenic poate induce calea de semnalizare AhR la pacienții cuboală cronică de rinichi[79]. În plus, șobolanii 5/6 Nx prezintă niveluri ridicate de chinurenină și 3-hidroxichinurenină serice și au reglat semnificativ expresia ARNm a AhR și CYP1A1 în țesutul osos în comparație cu șobolanii de control [80]. În special, nivelul seric de chinurenină, raportul seric chinurenină/triptofan și expresia ARNm AhR și CYP1A1 sunt mai scăzute la șobolanii de 3-luni 5/6 Nx comparativ cu 1-luni de 5/6 Nx. șobolani [80].
Activarea AhR mediază afectarea renală Calea AhR este activată înBoala cronică de rinichiPacienții cuBoala cronică de rinichisunt expuși la un nivel ridicat de toxine uremice, determinând un risc crescut de boli cardiovasculare. Mai multe toxine uremice, cum ar fi IS, IAA și IDG, sunt agonişti ai AhR. Cel mai recent studiu a demonstrat că AhR a fost activat la pacienții cuboală cronică de rinichistadiul 3 până la 5D [81]. Potențialul de activare a AhR (AhR-AP) se corelează puternic cu concentrația eGFR și IS. Expresia genelor țintă AHR din sânge, inclusiv CYP1A1 și AhRR, este reglată în sens pozitivBoala cronică de rinichipacienți comparativ cu martorii sănătoși [81]. Studii ulterioare au demonstrat că 5/6 șoareci nefrectomizați (5/6 Nx) au prezentat o creștere a AhR-AP seric și o inducere a expresiei ARNm CYP1A1 în inimă și aortă care au fost absente în AhR-/-Boala cronică de rinichisoareci [81]. Creșterea nivelului seric de AhR-AP și nivelul ARNm CYP1A1 reglat în sus în aorte și inimi de la șoarecii WT au fost observate după injecția în serie cu IS, dar nu și la șoarecii AhR-/- [81]. Luate împreună, aceste rezultate sugerează că calea de semnalizare AhR este activată atât la șoareci, cât și la pacienții cuboală cronică de rinichi.

Un alt studiu a demonstrat că substanțele dizolvate uremice indolice au reglat în sus expresia factorului tisular printr-o cale dependentă de AhR la pacienții cuboală cronică de rinichi(stadiile 3-5D) în comparație cu martorii sănătoși, evocând un efect „asemănător dioxinei”. Factorii tisulari crescuti au fost corelați pozitiv cu concentrațiile serice de IS și IAA la pacienții cuboală cronică de rinichi(etapele 3-5D) [74]. În HUVEC, tratamentul cu IS și IAA a reglat în continuare expresia a opt gene AhR: CYP1A1, CYP1B1, CYP1A2, factor de creștere transformator -3, prostaglandin G/H sintaza și ciclooxigenază, poli(ADP-riboză) polimerază inductibilă de CDD, receptorul 7 al chemokinei (motivul C-C) și AhRR, represorul AhR [74]. Implicarea activării AhR în producția de factor tisular a fost clarificată prin inhibarea siARN și cu inhibitorul AhR geldanamicina [74]. Aceste constatări au fost amplificate în celulele mononucleare din sângele periferic. Expresia și activitatea factorilor de țesut au fost, de asemenea, crescute de TCDD. În plus, nivelul IS este corelat semnificativ atât cu AhR, cât și cu activitățile factorului tisular la pacienții cu boală renală în stadiu terminal (IRST) [82]. IS activează calea AhR în celulele musculare netede vasculare aortice umane primare, iar AhR interacționează direct cu și stabilizează factorii de țesut. Antagonistul AhR inhibă factorul de țesut, crește ubiquitinarea și degradarea factorului de țesut și inhibă tromboza și leziunea endovasculară [82]. Mai mult decât atât, monocitele răspund la IS prin semnalizarea AhR și, în consecință, reglează expresia factorului de necroză tumorală-alfa la pacienții cu ESRD [83]. Luate împreună, aceste descoperiri indică faptul că activarea AhR este un mecanism cheie asociat cu boala cardiovasculară dăunătoare înboală cronică de rinichi.
Cu toate acestea, knockout-ul AhR duce la alterarea fenotipurilor renale și hepatice atât la șoareci, cât și la șobolani [84]. Șoarecii knockout AhR prezintă modificări ale funcției hepatice și ale canalului venos permeabil al ficatului. Șobolanii AhR-knockout prezintă modificări ale tractului urinar, inclusiv dilatare renală bilaterală (hidronefroză), modificări degenerative tubulare și uroepiteliale secundare și dilatare bilaterală a ureterului (hidroureter) [84]. Un alt studiu a indicat că hidrocarburile aromatice pot compensa funcția celulelor renale intervenind cu funcția mitocondrială și homeostazia glutationului și sunt implicate atât în populațiile mezenchimale, cât și în cele epiteliale în nefrotoxicitatea la această clasă eterogenă de substanțe chimice [85]. În plus, stimularea AhR poate reprezenta un efect renoprotector nou, care implică probabil mobilizarea și recrutarea de Treg și celule stem la rinichiul lezat [86].
Nivelul seric IS este între 7 și 343 μM (valoare medie: 120–140 μM) la pacienții cu hemodializă cronică [87]. IS circulă în forme libere și legate de albumină. La pacienții cu hemodializă, aproximativ 90% din IS este legat de proteinele serice, ceea ce indică faptul că nivelul seric liber IS este de 12 μM, un nivel eficient care duce în mare măsură la inducerea activității AhR în celulele cultivate [88]. Nivelul de IS este cel mai ridicat în rinichi și mai scăzut în plămâni, ficat și inimă la șobolanii nefrectomizați [89]. Șobolanii cu insuficiență renală cronică au prezentat niveluri de IS de șase ori mai mari în țesuturile renale și IS de 71 μM în omogenatul de rinichi. Dacă aceste constatări reflectă nivelul IS din țesutul renal la pacienții cu IRST, ar fi de așteptat ca AhR să fie complet activat și ca activarea AhR să sporească și mai mult expresia genelor țintă AhR, cum ar fi CYP1A1, CYP1A2, CYP1B1 și COX{{ 17}}. Un alt studiu a indicat că expresia proteinei CYP1A2 în rinichi și ficat a fost mult reglată la șobolani cu insuficiență renală cronică [90]. În plus, TCDD poate media hidronefroza la șoareci [91]. Toxicitatea TCDD este indusă exclusiv de AhR și, prin urmare, ar putea oferi indicii pentru efectele inhibitoare ale activității crescute a AhR mediate de niveluri ridicate de IS.
IS gratuit, nu IS legat de albumină, poate activa AhR. Un studiu a investigat efectul IS liber și legat de albumină asupra activării AhR utilizând nivelurile IS observate în diferite stadii ale pacienților cu boală cronică de rinichi. Un test reporter condus de AhR a arătat că ambele forme IS au mediat transcripția AhR dependentă de doză în celulele musculare netede vasculare [82]. Nivelul IS echivalent cu cel găsit în stadiile incipiente ale pacienților cu boală cronică de rinichi a crescut, de asemenea, transcripția AhR, care a fost inhibată în funcție de doză de antagonistul AhR CB7993113. În mod similar, IS a suprareglat expresia genelor țintă AhR endogene CYP1A1, CYP1A2 și AhRR, toate acestea fiind abrogate de antagonistul AhR [82]. Cu toate acestea, puține studii au examinat efectul IS asupra activității AhR în celulele tubulare proximale renale. Luate împreună, aceste rezultate arată că activitatea AhR reglată la nivelul rinichilor poate fi asociată cu nivelul ridicat de IS în boala renală.
Calea AhR este activată în nefropatia diabetică Nefropatia diabetică a devenit o mare problemă de sănătate globală. S-a raportat că activitatea de transactivare a AhR seric este mai mare la pacienții cu diabet de tip 2 cu nefropatie diabetică cu microalbuminurie, microalbuminurie și BRST decât la subiecții cu normoalbuminurie [92]. Liganzii AhR serici sunt corelați cu rata estimată de filtrare glomerulară (eGFR), nivelul creatininei serice, tensiunea arterială sistolica, hemoglobina glicata și durata diabetului. Activitatea ridicată de transactivare a AhR este un factor de risc independent în nefropatia diabetică [92]. Un studiu pe șoareci diabetici induși de streptozotocină a arătat că deficitul de AhR a redus inducerea COX-2/prostaglandinei E2, activitatea NADPH oxidazei, stresul oxidativ, peroxidarea lipidelor și N-Ɛ-carboximetil lizină [93]. N-Ɛ-carboximetil lizina a îmbunătățit semnificativ activitatea de legare la ADN AhR/COX-2, reciprocitatea proteină-ADN, reglarea genelor și acumularea de ECM în celulele tubulare proximale renale și celulele mezangiale, care ar putea fi inversate prin transfecția siRNA-AhR [93]. În plus, disfuncția rinichilor umani care apare ca urmare a nefropatiei diabetice a fost indicată pentru a duce la niveluri ridicate de IS seric [59].
AhR este asociat cu RAS
Sistemul renină-angiotensină (RAS) joacă un rol cheie în progresia bolii cronice de rinichi. Mai multe studii au indicat că AhR este asociat cu RAS. De exemplu, IS reduce expresia receptorului Mas în aortele șobolanilor normotensivi și hipertensivi [94]. Un alt studiu a demonstrat că IS a reglat în jos expresia receptorului Mas prin AhR/NF-kB și a mediat proliferarea celulară și exprimarea factorului tisular în celulele musculare netede aortice umane. Ang-(1-7) a suprimat expresia factorului tisular mediat de IS și proliferarea celulară prin inhibarea ERK1/2 și NF-kB fosforilate [94]. În plus, expresia receptorului Mas este reglată în jos în rinichii șobolanilor cu boală cronică de rinichi [95]. IS induce reglarea în jos a expresiei receptorului Mas prin calea de semnalizare OAT3/AhR/STAT3 în celulele tubulare proximale [95]. Reglarea descendentă mediată de IS a receptorului Mas este implicată în reglarea în sus a factorului de creștere transformator-beta 1 în celulele tubulare proximale. Un alt studiu a indicat că IS a indus expresia aortică a receptorului de prorenină și a reninei/proreninei prin absorbția indusă de transportorul de anioni organici 3-, producția de specii reactive de oxigen și activarea AhR și NF-κB p65 în celulele musculare netede vasculare [96]. Activarea indusă de IS a receptorului de prorenină promovează expresia factorului de țesut și proliferarea celulară în celulele musculare netede vasculare [96].
Calea AhR este activată în cancerele asociate sistemului urinar
Calea AhR este implicată în carcinogeneză [97]. S-a demonstrat că AhR se exprimă în principal în nucleele carcinomului renal cu celule clare (RCC) avansat și limfocitelor infiltrante tumorale, iar expresia sa se corelează cu stadiul tumorii patologice și cu gradul histologic [98]. Metaloproteinazele matriceale (MMP) aparțin unei familii de endopeptidaze dependente de zinc și sunt considerate ținte terapeutice pentru bolile renale [99]. Activarea AhR reglează în sus expresia ARNm a genelor sale țintă CYP1A1 și CYP1B1 și promovează invazia prin reglarea în sus a expresiei ARNm a MMP-1, MMP-2 și MMP-9 și prin reglarea în jos a expresiei ARNm a E. -caderina în liniile celulare RCC umane, inclusiv 786-O și ACHN [98]. În plus, un siARN pentru AhR a redus CYP-urile și a inhibat invazia celulelor canceroase însoțită de reglarea în jos a MMP în celulele 786-O [98]. Aceste constatări indică faptul că AhR reglează invazia celulelor RCC implicate în imunitatea tumorii. Același grup de studiu a arătat că expresia AhR nucleară a fost, de asemenea, semnificativ legată de stadiul T patologic, gradul histologic, invazia și implicarea ganglionilor limfatici la pacienții cu carcinom urotelial al tractului urinar superior [100]. Expresia AhR este considerată un predictor independent al supraviețuirii specifice bolii. Celulele T24 UC induse de TCDD au arătat expresia ARNm reglată în sus a AhR, CYP1A1 și CYP1B1 însoțită de expresia ARNm reglată în sus a MMP-1 și MMP{-9 și o invazie îmbunătățită a celulelor T24 [100]. Mai mult, celulele T24 transfectate cu un siARN pentru AhR au arătat expresia ARNm reglată în jos a AhR, CYP1A1, CYP1B1, MMP-1, MMP-2 și MMP{-9 și au indicat scăderea capacității de invazie [100]. Luate împreună, aceste constatări indică faptul că AhR joacă un rol important în invazivitatea celulelor canceroase și poate servi ca biomarker de prognostic și potențială țintă terapeutică pentru pacienții cu cancere asociate sistemului urinar.
Produse naturale, cum ar fi agoniştii AhR sau antagoniştii în bolile renale şi carcinomul cu celule renale
Polipeptidele transportoare de anioni organici și transportatorii de anioni organici joacă un rol cheie în eliminarea toxinei uremice renale. 4C1 (SLCO4C1) este singura polipeptidă care transportă anioni organici exprimată pe partea bazolaterală a celulelor tubulare proximale renale umane și modulează excreția de toxină uremică. Supraexpresia umană a SLCO4C1 în rinichii de șobolan promovează excreția renală a toxinei uremice și scade cardiomegalia, hipertensiunea și inflamația renală în insuficiența renală [101]. Statina induce expresia SLCO4C1 prin AhR prin legarea de XRE în regiunea sa promotor [101]. Administrarea de statine promovează eliminarea toxinelor uremice și atenuează afectarea organelor într-un model de insuficiență renală de șobolan. MicroARN joacă un rol important în mecanismul de apărare celulară. S-a raportat că miR-125b este activat transcripțional de Nrf2 și ar putea fi un inhibitor al represorului AhR la șoarecii induși de cisplatină, ceea ce contribuie la protejarea rinichiului de leziuni renale acute [102].
Produsele naturale din clinică au fost considerate ca o terapie alternativă pentru prevenirea și tratarea unei multitudini de boli în întreaga lume [103–107]. Produsele naturale continuă, de asemenea, să ofere o sursă proteică și unică de noi candidați bioactivi pentru descoperirea medicamentelor [108-115]. Numeroase studii au demonstrat o varietate de compuși naturali derivați din produse care pot activa sau inhiba direct AhR [116–119]. Încă din anii 1970, mai multe studii au raportat că liganzii AhR din extractele vegetale sau materialele derivate din legume mediază activitatea CYP1A1 [120, 121]. După cum se arată în figura 3, membrii familiei cruciferelor, cum ar fi broccoli, varza de Bruxelles, varza albă și conopida, au surse bogate de glucobrassicină sau conjugați de glucozinolat care produc indol-3-carbinol (I3C) și indol{{ 16}}acetonitril (I3AC) prin utilizarea clivajului enzimatic în timpul masticației [122, 123]. I3C și I3AC se pot lega și activa AhR. Indolo[3,2,-b]carbazol (ICZ) și 3,3′-diindolil metan (DIM) sunt doi produși majori de condensare acidă ai I3C. ICZ are o afinitate mai mare pentru ligandul AhR în comparație cu alte produse naturale [124]. 3,3′-Diindolilmetan este un agonist AhR stabilit [124]. Conjugații de glucozinolat pot activa AhR la șoareci și oameni [121, 125]. După consum, glucozinolații suferă hidroliză, transferând I3C, ICZ, DIM și ([2-(indol-3-ilmetil)-indol{-3-il]indol-3-ilmetan (LTr1) , care servesc ca agonisti AhR [121].Acești compuși sunt implicați în expresia AhR intestinală necesară pentru menținerea celulelor limfoide înnăscute și a limfocitelor intraepiteliale.Aceste descoperiri demonstrează o legătură importantă între factorii dietetici, AhR și imunitatea intestinală. Ulterior, studiile au demonstrat că mai mulți compuși din produse naturale, cum ar fi I3C, curcumină, quercetină, resveratrol, 7,8-dihidrorutacarpină, dibenzoil metan și carotenoizi (canthaxantina, astaxantina și -apo-8′-carotenal) ar putea se leagă competitiv la AhR și/sau mediază expresia genelor dependente de AhR [116, 117, 123, 126].
Polifenolii sunt compuși larg răspândiți în întregul regn vegetal [127]. Se caracterizează prin utilizarea unei structuri chimice clasice de inel fenol. În funcție de cantitățile de inele fenolice din compuși și de abordarea pe care o utilizează, polifenolii sunt împărțiți în 5 categorii: flavonoide, acizi fenolici, stilbeni, lignani și taninuri [128]. Flavonoidele și acizii fenolici sunt cei mai abundenți polifenoli din dieta zilnică și pot fi împărțiți în mai multe categorii în funcție de gradul de oxidare al heterociclului de oxigen, inclusiv flavonoli, flavonoli, flavanone, flavone, izoflavone, proantocianidine și antocianine [128]. Flavonoidele din produsele naturale constituie cea mai mare categorie de liganzi AhR [117, 129, 130]. Flavonoidele, cum ar fi kaempferol, (–)-epigallocatechin galat, luteolina, miricetina, epigalocatechin, morin, galangin, eriodictyol, tangeritin, apigenin și naringenin, sunt în mare parte antagoniști AhR, dar unii dintre ei, inclusiv chrysin, baitincalein, dios quer , icariina, tangeritina și tamarixetina sunt agonişti AhR [116, 117, 126]. Pe lângă interacțiunea cu AhR, multe flavonoide sunt, de asemenea, substraturi pentru CYP1A1. Aceste flavonoide sunt larg distribuite în plante medicinale, fructe, legume și ceaiuri, iar concentrațiile de flavonoide din sângele uman sunt în intervalul micromolar scăzut, niveluri suficiente pentru a inhiba/activa AhR [116]. Astfel, nu este surprinzător faptul că extractele multor produse naturale prezintă activitate de agonist și/sau antagonist AhR. Prin urmare, produsele naturale includ în mod obișnuit liganzi AhR sau produse naturale care pot fi transformate în liganzi AhR și, ca atare, flavonoidele sunt cea mai mare clasă de liganzi AhR naturali care sunt disponibili pentru oameni și animale. Dovezile tot mai mari au demonstrat că polifenolii, în special flavonoidele, ca modulatori ai AhR, sunt utilizați pe scară largă pentru reglarea sistemului imunitar intestinal și tratamentul tumorilor [116–118, 131, 132], dar doar câteva studii au raportat că produsele naturale reglează AhR. în afectarea rinichilor.
Acizii aristolohici, precum acidul aristolohic I (AAI) și acidul aristolohic II, cu structura acizilor nitrofenoltren carboxilici, sunt componenta activă principală a speciilor Aristolochia [133]. Se știe că acizii aristolohici posedă proprietăți antiinflamatorii până când a fost găsită prima cauză a nefropatiei în Belgia, care este acum considerată nefropatie a acidului aristolohic (AAN) [134].
Expunerea la AA a fost recent implicată în nefropatia endemică balcanică și asociată cu cancerul urotelial [135, 136]. Mecanismul a evidențiat că nefrotoxicitatea mediată de AAI este asociată cu deficit de NADPH-citocrom P450 reductază specific ficatului, iar inducerea CYP1A scade semnificativ toxicitatea renală indusă de AAI [134]. Baicalinul atenuează semnificativ toxicitatea renală mediată de AAI prin inducerea CYP1A1 și CYP1A2 dependentă de AhR în ficat [137]. Tanshinona I promovează metabolismul AAI și previne leziunea renală mediată de AAI prin inducerea in vivo a CYP1A1 și CYP1A2 hepatic [138].
Cistancheeste unul dintre cele nouă medicamente nemuritoare pentru boala cronică de rinichi
A fost înregistrat ca un material medicinal hrănitor de calitate din cele mai vechi timpuri. Și a fost folosit ca ingredient medicinal în istoria umanității de mai bine de 2,000 ani. poate promova proliferarea celulelor renale și poate reduce apoptoza celulelor renale.Cistancheare efecte de revigorare a rinichilor, tratarea infecțiilor renale, tratarea nefritei și insuficiența renală. Pe baza eficacității sale, a fost utilizat pe scară largă în industria medicală, medicală și cosmetică.
Concluzii finale
Inițial, AhR a fost descoperit ca o moleculă de semnalizare cu detecție chimică care a mediat răspunsurile toxice de la poluanții de mediu. În ultimii ani, studiile în creștere asupra liganzilor AhR au mărturisit o expansiune fără egal de la răspunsurile toxice exogene la multe domenii legate de biologii și medicină, cum ar fi cancerul, reglarea imunității, bolile cardiovasculare și bolile de rinichi, semnalizarea AhR prezintă o varietate de funcții biologice. care și-au extins funcția transcripțională clasică în reglarea căii de semnalizare citosolică și posedă noi liganzi endogeni care se pot lega și activa expresia genei dependente de AhR. Deși liganzii AhR raportați recent s-au extins foarte mult, multe studii conexe ale AhR sunt încă riguros provocatoare și ar trebui depuse eforturi mari în viitor.
În primul rând, identificarea structurală a liganzilor AhR ar putea oferi o perspectivă asupra noilor liganzi exogeni și endogeni ai AhR, deși abordările de fracționare a probelor biologice nu au putut identifica mulți liganzi endogeni în trecut, cea mai recentă dezvoltare a abordărilor metabolomice cu randament ridicat, rapide și sensibile oferă căi pentru identificarea, izolarea și caracteristicile noilor liganzi AhR din urme de matrice complexe și probe biologice. Metabolomica și lipidomica au fost utilizate cu succes pentru a descoperi și identifica o varietate de noi liganzi endogeni AhR, în special metaboliți care conțin hidrocarburi aromatice (toxine uremice), atât la modele animale, cât și la pacienții cu boală cronică de rinichi [50,139-143). În general, caracterizarea spectrului de liganzi endogeni AhR va oferi noi mecanisme moleculare și biochimice prin care liganzii pot induce activarea AhR.
În al doilea rând, produsele naturale au fost utilizate pe scară largă pentru prevenirea și intervenția unei multitudini de boli în întreaga lume. Anchetatorii au dezvăluit o tendință intrigantă în dezvoltarea medicamentelor începând cu secolul al II-lea: o întoarcere la natură ca sursă de agenți potențiali noi [144,145]. Produsele naturale au o gamă largă de bioactivități și au fost o sursă continuă de noi medicamente care au contribuit la aproximativ 46% din medicamentele aprobate de Food and Drug Administration din 1981 până în 2014 [146-149]. Studiile menționate mai sus au demonstrat că flavonoidele sunt antagonişti sau agonişti AhR. Flavonoidele sunt distribuite pe scară largă în produse naturale, cum ar fi plantele medicinale, fructele, legumele și ceaiurile. Până în prezent, mai mult de 15,000 flavonoide au fost identificate din produse naturale[150]. Datorită importanței lor în reglarea activității AhR, ar trebui depuse eforturi mari pentru a investiga în continuare reglarea flavonoidelor asupra activității AhR. O mai bună înțelegere a structurilor lor chimice și a activității biologice AhR va fi importantă pentru a descoperi potențialul lor suplimentar ca medicamente terapeutice și mecanismul lor molecular.
În al treilea rând, toxinele uremice din metabolismul triptofanului și dioxinele din poluanții mediului activează calea de semnalizare AhR. Aceste toxine induc activarea leucocitelor și disfuncția endotelială, provocând tromboză și inflamație, precum și creșterea stresului oxidativ vascular. Toxinele uremice din metabolismul triptofanului care activează AhR explică modul în care aceste toxine contribuie la BCV la pacienții cu boală cronică de rinichi. Aceste mecanisme de toxicitate a toxinelor uremice pot oferi noi abordări terapeutice potențiale care vizează activarea AhR. Deși mai multe experimente au explorat relația dintre activitatea AhR și diferite boli de rinichi prin analizarea genelor țintă ale AhR atât la modele animale, cât și la pacienții cu boală cronică de rinichi, AhR în boala renală este încă la început în comparație cu cancerul și boala imună. Un număr mare de metaboliți, în special toxine uremice, au fost identificați prin metabolomice cu randament ridicat, deși numărul este insuficient. Ar trebui efectuate studii suplimentare asupra efectului metaboliților noi asupra activității AhR. În plus, calea AhR poate interacționa cu Wnt/-catenina, factorul de creștere transformator-/proteina morfogenetică osoasă și căile de semnalizare Notch, precum și căile receptorului tirozin kinazei, inclusiv receptorul factorului de creștere endotelial vascular, receptorul factorului de creștere al keratinocitelor și creșterea epidermică. receptor de factor, în mai multe boli umane [118]. Multe studii au documentat bine că factorul de creștere transformator-/proteina morfogenetică osoasă, Wnt/-catenina, semnalizarea Notch și căile receptorilor tirozin kinazei sunt implicate în boala cronică de rinichi[151,152]. Puține studii au demonstrat dacă AhR poate interacționa cu aceste căi de semnalizare în bolile de rinichi.
În cele din urmă, indiferent de aplicațiile translaționale și clinice promițătoare ale AhR, majoritatea cunoștințelor disponibile în prezent despre funcția sa fiziopatologică au fost demonstrate prin utilizarea modelelor animale, care au condus la anumite limitări pentru transferul direct al realizărilor la pacienți. Un mare efort se va concentra cu siguranță pe validarea datelor de la experimentele pe animale până la aplicarea clinică în viitor, iar biologia sistemului, inclusiv genomica, transcriptomica, proteomica, metabolomica și lipidomica, va juca cel mai probabil un rol important în studiile asupra AhR. Acestea sunt domenii interesante pentru studii viitoare. Este foarte probabil ca studiile viitoare să ofere noi abordări de diagnostic și prognostic pentru bolile umane complexe și să stabilească noi strategii terapeutice care vizează activarea AhR.

cistanchepoate satrata bolile de rinichi imbunatateste functia renala
Finanțarea
Acest studiu a fost susținut de Fundația Națională pentru Științe Naturale din China (Nos81673578,8187298S5).
Disponibilitatea datelor și materialelor
Nu se aplică
Aprobarea etică și acordul de participare
Nu se aplică
Consimțământ pentru publicare
Nu se aplică
Interese concurente
Autorii dezbat faptul că au interese concurente
Referințe
1. Denison MS, Nagy SR. Activareareceptor de hidrocarburi ariide substanțe chimice exogene și endogene structural diverse. Annu Rev Pharmacol Toxicol. 2003;43:309–34.
2. Roger HM, Licht TR. Cataboliți microbieni de triptofan în sănătate și boală. Nat Commun. 2018;9:3294.
3. Tete A, Gallais I, Imran M, Chevonne M, Liamin M, Sparfel L, Bucher S, Burel A, Podechard N, Appenzeller BMR, et al. Mecanisme implicate în moartea hepatocitelor steatotice WIF-B9 co-expuse la benzo[a]piren și etanol: un posibil rol cheie pentru metabolismul xenobiotic și oxidul nitric. Free Radic Biol Med. 2018;129:323–37.
4. Denison MS, Vella LM. Receptorul hepatic Ah pentru 2,3,7,8-tetrarh-rodibenzo-p-dioxină: diferențele dintre specii în disocierea subunităților. Arch Biochem Biophys. 1990;277:382–8.
5. Das DN, Naik PP, Mukhopadhyay S, Panda PK, Sinha N, Meher BR, Bhutia SK. Eliminarea mitocondriilor disfuncționale prin mitofagie suprimă apoptoza indusă de benzo[a]piren. Free Radic Biol Med. 2017;112:452–63.
6. Forman HJ, Finch CE. O revizuire critică a testelor pentru componentele periculoase ale poluării aerului. Free Radic Biol Med. 2018;117:202–17.
7. Hankinson O. Thereceptor de hidrocarburi ariicomplex. Annu Rev Pharmacol Toxicol. 1995;35:307–40.
8. Yamamura K, Uruno T, Shiraishi A, Tanaka Y, Ushijima M, Nakahara T, Watanabe M, Kido-Nakahara M, Tsuge I, Furue M, Fukui Y. Factorul de transcripție EPAS1 leagă deficiența DOCK8 de inflamația atopică a pielii prin IL -31 inducție. Nat Commun. 2017;8:13946.
9. Endo Y, Yokote K, Nakayama T. The obezity-related pathology and Th17 cells. Cell Mol Life Sci. 2017;74:1231–45.
10. Xia P, Liu J, Wang S, Ye B, Du Y, Xiong Z, Han ZG, Tong L, Fan Z. WASH menține celulele NKp46 (plus) ILC3 prin promovarea expresiei AHR. Nat Commun. 2017;8:15685.
11. Kalthof S, Landerer S, Reich J, Strassburg CP. Efectele protectoare ale cafelei împotriva stresului oxidativ indus de carcinogenul din tutun, benzo[alfa]piren. Free Radic Biol Med. 2017;108:66–76.
12. Sinclair LV, Neyens D, Ramsay G, Taylor PM, Cantrell DA. Analiza unicelulare a chinureninei și a transportului de aminoacizi a sistemului L în celulele T. Nat Commun. 2018;9:1981.
13. Venken K, Jacques P, Mortier C, Labbadia ME, Decruy T, Coudenys J, Hoyt K, Wayne AL, Hughes R, Turner M și colab. Inhibarea RORgammat vizează selectiv IL-17 producătoare de iNKT și celule gamma-delta-T îmbogățite la pacienții cu spondiloartrită. Nat Commun. 2019;10:9.
14. Singh R, Chandrashekharappa S, Bodduluri SR, Baby BV, Hegde B, Kotla NG, Hiwale AA, Saiyed T, Patel P, Vijay-Kumar M și colab. Îmbunătățirea integrității barierei intestinale de către un metabolit microbian prin calea Nrf2. Nat Commun. 2019;10:89.
15. Sampath C, Sprouse JC, Freeman ML, Gangula PR. Activarea Nrf2 atenuează golirea gastrică întârziată la șoarecii femele cu diabet zaharat indus de obezitate (T2DM). Free Radic Biol Med. 2019;135:132–43.
16. Wang GZ, Zhang L, Zhao XC, Gao SH, Qu LW, Yu H, Fang WF, Zhou YC, Liang F, Zhang C și colab. Thereceptor de hidrocarburi ariimediază expresia PD-L1 indusă de tutun și este asociată cu răspunsul la imunoterapie. Nat Commun. 2019;10:1125.
17. Jaeger C, Tischkau SA. Rolulreceptor de hidrocarburi ariiîn perturbarea ceasului circadian și disfuncția metabolică. Environ Health Insights. 2016;10:133–41.
18. Zhang L, Nichols RG, Correll J, Murray IA, Tanaka N, Smith PB, Hubbard TD, Sebastian A, Albert I, Hatzakis E și colab. Poluanții organici persistenți modifică homeostazia metabolică a microbiotei intestinale la șoareciactivarea receptorului de hidrocarburi arii. Perspectivă pentru sănătatea mediului. 2015;123:679–88.
19. Brokken LJ, Lundberg PJ, Spano M, Manicardi GC, Pedersen HS, Strucinski P, Goralczyk K, Zviezdai V, Jonsson BA, Bonde JP și colab. Interacțiuni între polimorfisme înreceptor de hidrocarburi ariicalea de semnalizare și expunerea la poluanți organoclori persistenti afectează calitatea spermei umane. Reprod Toxicol. 2014;49:65–73.
20. Kim YC, Seok S, Byun S, Kong B, Zhang Y, Guo G, Xie W, Ma J, Kemper B, Kemper JK. AhR și SHP reglează nivelurile de fosfatidilcolină și S-adenozil-metionină în ciclul cu un singur carbon. Nat Commun. 2018;9:540.
21. Phelan D, Winter GM, Rogers WJ, Lam JC, Denison MS. Activarea căii de transducție a semnalului receptorului Ah de către bilirubină și biliverdină. Arch Biochem Biophys. 1998;357:155–63.
22. Flaveny CA, Murray IA, Chiaro CR, Perdew GH. Selectivitatea ligandului și reglarea genelor de către omreceptor de hidrocarburi ariila şoarecii transgenici. Mol Pharmacol. 2009;75:1412–20.
23. Nicholson JK, Lindon JC, Holmes E. „Metabonomics”: înțelegerea răspunsurilor metabolice ale sistemelor vii la stimuli patofiziologici prin analiza statistică multivariată a datelor spectroscopice RMN biologice. Xenobiotica. 1999;29:1181–9.
24. Scheubert K, Hufsky F, Petras D, Wang M, Nothias LF, Duhrkop K, Bandeira N, Dorrestein PC, Bocker S. Signifcance estimation for large scale metabolomics adnotations by spectral matching. Nat Commun. 2017;8:1494.
25. Zhao YY, Cheng XL, Vaziri ND, Liu S, Lin RC. Aplicații metabonomice bazate pe UPLC pentru descoperirea biomarkerilor bolilor în chimia clinică. Clin Biochem. 2014;47:16–26.
26. Zhao YY, Miao H, Cheng XL, Wei F. Lipidomics: o nouă perspectivă asupra mecanismului biochimic al metabolismului lipidelor și al bolii asociate dereglării. Chem Biol Interact. 2015;240:220–38.
27. Zhao YY, Cheng XL, Lin RC, Wei F. Aplicații lipidomice pentru descoperirea biomarkerilor de boală în modele de mamifere. Biomark Med. 2015;9:153–68.
28. Chen DQ, Chen H, Chen L, Tang DD, Miao H, Zhao YY. Aplicație metabolomică în evaluarea toxicității și identificarea biomarkerului toxicologic al produsului natural. Chem Biol Interact. 2016;252:114–30.
29. Gar C, Rottenkolber M, Prehn C, Adamski J, Seissler J, Lechner A. Aminoacizii din ser și plasmă ca markeri ai prediabetului, rezistenței la insulină și diabetului incident. Crit Rev Clin Lab Sci. 2018;55:21–32.
30. Chen H, Miao H, Feng YL, Zhao YY, Lin RC. Metabolomica în dislipidemie. Adv Clin Chem. 2014;66:101–19.
31. Zhao YY, Cheng XL, Lin RC. Aplicații lipidomice pentru descoperirea biomarkerilor bolilor în chimia clinică. Int Rev Cell Mol Biol.2014;313:1–26.
32. Zhao YY, Wu SP, Liu S, Zhang Y, Lin RC. Cromatografia lichidă ultra-performantă-spectrometria de masă este o tehnologie sensibilă și puternică în aplicațiile lipidomice. Chem Biol Interact. 2014;220:181–92.
33. Zhao YY, Lin RC. Aplicația UPLC-MSE în descoperirea biomarkerilor de boală: descoperirile din proteomică la metabolomică. Chem Biol Interact. 2014;215:7–16.
34. Earl DC, Ferrell PB Jr, Leelatian N, Froese JT, Reisman BJ, Irish JM, Bach Mann BO. Descoperirea moleculelor efectoare selective ale celulelor umane folosind metabolomica cu activitate multiplexată cu o singură celulă. Nat Commun. 2018;9:39.
.
35. Park KS, Xu CL, Cui X, Tsang SH. Reprogramarea metabolomului salvează degenerarea retinei. Cell Mol Life Sci. 2018;75:1559–66.
36. Hayton S, Maker GL, Mullaney I, Trengove RD. Design experimental și standarde de raportare pentru studiile metabolomice ale liniilor celulare de mamifere. Cell Mol Life Sci. 2017;74:4421–41.
37. Deidda M, Piras C, Cadeddu Dessalvi C, Conga D, Locci E, Ascedu F, De Candia G, Cadeddu M, Lai G, Pirisi R, et al. Amprenta metabolomică a sângelui este distinctă în boala coronariană și steno sănătoasă sau în boala cardiacă ischemică microvasculară. J Transl Med. 2017;15:112.
38. Zhao YY, Cheng XL, Cui JH, Yan XR, Wei F, Bai X, Lin RC. Efectul Agosta 4,6,8(14),22-terrain-3-one (unu) asupra șobolanului insuficienței renale cronice indusă de adenină: un studiu metabonomic seric bazat pe cromatografie lichidă ultra-performanță/high- spectrometrie de masă de sensibilitate cuplată cu algoritmul MassLynx i-FIT. Clin Chim Acta. 2012;413:1438–45.
39. Zhao YY, Li HT, Feng YI, Bai X, Lin RC. Studiu metabonomic urinar al stratului de suprafață al Poria cocos ca tratament eficient pentru leziuni renale cronice la șobolani. J Etnofarmacol. 2013;148:403–10.
40. Zhao YY, Lei P, Chen DQ, Feng YL, Bai X. Profilul metabolic renal al leziunii renale precoce și efectele renoprotective ale epidermei Poria cocos folosind UPLC Q-TOF/HSMS/MSE. J Pharm Biomed Anal. 2013;81–82:202–9.
41. Chen DQ, Cao G, Chen H, Argyopoulos CP, Yu H, Su W, Chen L, Samuels DC, Zhuang S, Bayliss GP și colab. Identificarea metaboliților serici asociați cu progresia bolii renale cronice și cu efectul antifibrotic al 5-metoxitriptofanului. Nat Commun. 2019;10:1476.
42. Zhao YY. Metabolomica în boala cronică de rinichi. Clin Chim Acta. 2013;422:59–69.
43. Chen H, Chen L, Liu D, Chen DQ, Vaziri ND, Yu XY, Zhang L, Su W, Bai X, Zhao YY. Fenotipul clinic combinat și analiza lipidomică dezvăluie impactul bolii cronice de rinichi asupra metabolismului lipidic. J Proteome Res. 2017;16:1566–78.
44. Chen DQ, Chen H, Chen L, Vaziri ND, Wang M, Li XR, Zhao YY. Legătura dintre fenotip și metabolismul acizilor grași în boala renală cronică avansată. Transplant Nephrol Dial. 2017;32:1154–66.
45. Chen H, Cao G, Chen DQ, Wang M, Vaziri ND, Zhang ZH, Mao JR, Bai X, Zhao YY. Perspectivele metabolomice asupra semnalizării redox activate și a disfuncției metabolismului lipidic în progresia bolii renale cronice. Redox Biol. 2016;10:168–78.
46. Zhang ZH, Mao JR, Chen H, Su W, Zhang Y, Zhang L, Chen DQ, Zhao YY, Vaziri ND. Îndepărtarea produselor de retenție uremică prin hemodializă este cuplată cu pierderea nediscriminată a metaboliților vitali. Clin Biochem. 2017;50:1078–86.
47. Bridal F, Le Lay A, Dumas ME, Gauguier D. Implicația metaboliților microbiotei intestinale în bolile cardiovasculare și metabolice. Cell Mol Life Sci. 2018;75:3977–90.
48. Chen DQ, Cao G, Chen H, Liu D, Su W, Yu XY, Vaziri ND, Liu XH, Bai X, Zhang L, Zhao YY. Expresiile genelor și proteinelor și metabolomica prezintă semnalizare redox activată, iar calea Wnt/-catenină este asociată cu disfuncția metabolitului la pacienții cu boală cronică de rinichi. Redox Biol. 2017;12:505–21.
49. Feng YL, Chen H, Chen DQ, Vaziri ND, Su W, Ma SX, Shang YQ, Mao JR, Yu XY, Zhang L și colab. Căile activate NF-κB/Nrf2 și Wnt/-catenina sunt asociate cu metabolismul lipidic la pacienții cu boală renală cronică cu microalbuminurie și macroalbuminurie. Biochim Biophys Acta Mol Basis Dis. 2019;1865:2317–32.
50. Zhao YY, Cheng XL, Wei F, Xiao XY, Sun WJ, Zhang Y, Lin RC. Studiul metabonomic seric al insuficienței renale cronice induse de adenină la șobolani prin cromatografie lichidă ultra-performanță cuplată cu spectrometrie de masă cu timp de zbor quadrupol. Biomarkeri. 2012;17:48–55.
51. Vanholder R, De Smet R, Glorieux G, Argiles A, Bauermeister U, Brunet P, Clark W, Cohen G, De Deyn PP, Deppisch R și colab. Revizuirea toxinelor uremice: clasificare, concentrație și variabilitate interindividuală. Rinichi Int. 2003;63:1934–43.
52. Duranton F, Cohen G, De Smet R, Rodriguez M, Jankowski J, Vanholder R, Argiles A. Concentrații normale și patologice ale toxinelor uremice. J Am Soc Nephrol. 2012;23:1258–70.
53. Dolivo DM, Larson SA, Dominko T. Metaboliții triptofanului, chinurenina și serotonina, reglează activarea fibroblastelor și fibroza. Cell Mol Life Sci. 2018;75:3663–81.
54. Song P, Ramprasath T, Wang H, Zou MH. Calea anormală a chinureninei a catabolismului triptofanului în bolile cardiovasculare. Cell Mol Life Sci. 2017;74:2899–916.
55. Fatokun AA, Hunt NH, Ball HJ. Indoleamină 2,3-dioxigenaza 2 (IDO2) și calea chinureninei: caracteristici și roluri potențiale în sănătate și boală. Aminoacizi. 2013;45:1319–29.
56. Liu Y, Liang X, Yin X, Lv J, Tang K, Ma J, Ji T, Zhang H, Dong W, Jin X și colab. Blocarea circuitelor metabolice IDO kinurenine-AhR abrogă repausul imunologic indus de IFN- -a celulelor care repopulează tumorile. Nat Commun. 2017;8:15207.
57. Santoro A, Ostan R, Candela M, Biagi E, Brigidi P, Capri M, Franceschi C. Modificări ale microbiotei intestinale în deceniile extreme ale vieții umane: un focus pe centenarii. Cell Mol Life Sci. 2018;75:129–48.
58. Li G, Young KD. Producția de indol de către triptofanaza TnaA în Escherichia coli este determinată de cantitatea de triptofan exogen. Microbiologie. 2013;159:402–10.
59. Schroeder JC, Dinatale BC, Murray IA, Flaveny CA, Liu Q, Laurenzana EM, Lin JM, Strom SC, Omiecinski CJ, Amin S, Perdew GH. Toxina uremică 3-indoxil sulfatul este un agonist endogen puternic pentru om.receptor de hidrocarburi arii. Biochimie. 2010;49:393–400.
60. Addi T, Dou L, Burley S. Tryptophan-derived uremic toxins and thrombosis in chronic kidney disease. Toxine. 2018;10:412.
61. Jin UH, Lee SO, Sridharan G, Lee K, Davidson LA, Jayaraman A, Chapkin RS, Alaniz R, Safe S. Metaboliții triptofan derivati din microbiom și ai acestorareceptor de hidrocarburi arii-activităţi agoniste şi antagoniste dependente. Mol Pharmacol. 2014;85:777–88.
62. Hubbard TD, Murray IA, Bisson WH, Lahoti TS, Gowda K, Amin SG, Patterson AD, Perdew GH. Adaptarea omuluireceptor de hidrocarburi ariipentru a simți indolii derivați din microbiotă. Sci Rep. 2015;5:12689.
63. Weems JM, Yost GS. 3-Meboliții metilindol induc enzimele pulmonare CYP1A1 și CYP2F1 prin mecanisme AhR și, respectiv, non-AhR. Chem Res Toxicol. 2010;23:696–704.
64. Rooks MG, Garrett WS. Microbiota intestinală, metaboliți și imunitatea gazdei. Nat Rev Immunol. 2016;16:341–52.
65. Li DY, Tang WHW. Rolul contributiv al microbiotei intestinale și al metaboliților acestora la complicațiile cardiovasculare în boala cronică de rinichi. Semin Nefrol. 2018;38:193–205.
66. Vaziri ND, Wong J, Pahl M, Piceno YM, Yuan J, DeSantis TZ, Ni Z, Nguyen TH, Andersen GL. Boala cronică de rinichi alterează forurile microbiene intestinale. Rinichi Int. 2013;83:308–15.
67. Chen YY, Chen DQ, Chen L, Liu JR, Vaziri ND, Guo Y, Zhao YY. Microbiomul-metabolomul dezvăluie contribuția axei intestin-rinichi la bolile de rinichi. J Transl Med. 2019;17:5.
68. Feng YL, Cao G, Chen DQ, Vaziri ND, Chen L, Zhang J, Wang M, Guo Y, Zhao YY. Microbiomul-metabolomica dezvăluie microbiota intestinală asociată cu metaboliții conjugați cu glicină și metabolismul poliaminei în boala cronică de rinichi. Cell Mol Life Sci. 2019.
69. Chen L, Chen DQ, Liu JR, Zhang J, Vaziri ND, Zhuang S, Chen H, Feng YL, Guo Y, Zhao YY. Obstrucția ureterală unilaterală provoacă disbioză microbiană intestinală și tulburări metabolom care contribuie la fibroza tubulointerstițială. Exp Mol Med. 2019;51:38.
70. Iu M, Zago M, Rico de Souza A, Bouttier M, Pareek S, White JH, Hamid Q, Eidelman DH, Baglole CJ. RelB atenuează apoptoza indusă de extractul de fum de țigară în asociere cu reglarea transcripțională areceptor de hidrocarburi arii. Free Radic Biol Med. 2017;108:19–31.
71. Moura-Alves P, Fae K, Houthuys E, Dorhoi A, Kreuchwig A, Furkert J, Barison N, Diehl A, Munder A, Constant P, et al. Sentirea AhR a pigmenților bacterieni reglează apărarea antibacteriană. Natură. 2014;512:387–92.
72. Brito JS, Borges NA, Esgalhado M, Magliano DC, Soulage CO, Mafra D.Receptor de hidrocarburi ariiactivarea în boala cronică de rinichi: rolul toxinelor uremice. Nefron. 2017;137:1–7.
73. Sallee M, Dou L, Cerini C, Poitevin S, Brunet P, Burtey S. Thereceptor de hidrocarburi arii-efectul de activare al toxinelor uremice din metabolismul triptofanului: un nou concept pentru a înțelege complicațiile cardiovasculare ale bolii cronice de rinichi. Toxine. 2014;6:934–49.
74. Gondolin B, Cerini C, Dou L, Sallee M, Duval-Sabatier A, Pletinck A, Calaf R, Lacroix R, Jourde-Chiche N, Poitevin S, et al. Substanțele dizolvate uremice indolice cresc producția de factor tisular în celulele endoteliale de cătrereceptor de hidrocarburi ariicalea. Rinichi Int. 2013;84:733–44.
75. Ichii O, Otsuka-Kanazawa S, Nakamura T, Ueno M, Kon Y, Chen W, Rosenberg AZ, Kopp JB. Leziuni ale podocitelor cauzate de sulfatul de indoxil, o toxină uremică și ligand al receptorilor aril-hidrocarburi. Plus unu. 2014;9:e108448.
76. Hamano H, Ikeda Y, Watanabe H, Horinouchi Y, Izawa-Ishizawa Y, Imanishi M, Zamami Y, Takechi K, Miyamoto L, Ishizawa K și colab. Toxina uremică indoxil sulfatul interferează cu metabolismul fierului prin reglarea hepcidinei în boala cronică de rinichi. Transplant Nephrol Dial. 2018;33:586–97.
77. Watanabe I, Tatebe J, Namba S, Koizumi M, Yamazaki J, Morita T. Activarea receptorului de hidrocarburi arii mediază expresia proteinei chemoatractante monocite induse de sulfat de indoxil-1 în celulele endoteliale ale venei ombilicale umane. Circ J. 2013;77:224–30.
78. Dou L, Sallee M, Cerini C, Poitevin S, Gondouin B, Jourde-Chiche N, Fal‑ lague K, Brunet P, Calaf R, Dussol B și colab. Efectul cardiovascular al acidului indol-3 solut uremic. J Am Soc Nephrol. 2015;26:876–87.
79. Schefold JC, Zeden JP, Fotopoulou C, von Haehling S, Pschowski R, Hasper D, Volk HD, Schuett C, Reinke P. Activitate crescută de indoleamină 2,3-dioxigenază (IDO) și niveluri serice crescute de triptofan cataboliți la pacienții cu boală cronică de rinichi: o posibilă legătură între inflamația cronică și simptomele uremice. Transplant Nephrol Dial. 2009;24:1901–8.
80. Kalaska B, Pawlak K, Domaniewski T, Oksztulska-Kolanek E, Znorko B, Roszczenko A, Rogalska J, Brzoska MM, Lipowicz P, Doroszko M, et al. Niveluri crescute de chinurenină periferică scad rezistența oaselor la șobolanii cu boală cronică de rinichi. Fata Physiol. 2017;8:836.
81. Dou L, Poitevin S, Sallee M, Addi T, Gondolin B, McKay N, Denison MS, Jourde-Chiche N, Duval-Sabatier A, Cerini C și colab. Receptorul de hidrocarburi arii este activat la pacienții și șoarecii cu boală cronică de rinichi. Rinichi Int. 2018;93:986–99.
82. Shivanna S, Kolandaivelu K, Shashar M, Belghasim M, Al-Rabadi L, Bal‑cells M, Zhang A, Weinberg J, Francis J, Pollastri MP și colab. Receptorul de hidrocarburi arii este un regulator critic al stabilității factorului de țesut și o țintă antitrombotică în uremie. J Am Soc Nephrol. 2016;27:189–201.
83. Kim HY, Yoo TH, Hwang Y, Lee GH, Kim B, Jang J, Yu HT, Kim MC, Cho JY, Lee CJ și colab. Disfuncția imună mediată de indoxil sulfat (IS) provoacă leziuni endoteliale la pacienții cu boală renală în stadiu terminal (IRST). Sci Rep. 2017;7:3057.
84. Harrill JA, Hukkanen RR, Lawson M, Martin G, Gilger B, Soldatow V, Lecluyse EL, Budinsky RA, Rowlands JC, Thomas RS. Eliminarea receptorului de hidrocarburi arii are ca rezultat fenotipuri hepatice și renale distincte la șobolani și șoareci. Toxicol Appl Pharmacol. 2013;272:503–18.
85. Parrish AR, Alejandro NF, Bowes Iii RC, Ramos KS. Profiluri de răspuns citotoxice ale celulelor epiteliale și mezenchimale renale cultivate la hidrocarburi aromatice selectate. Toxicol in vitro. 1998;12:219–32.
86. Baban B, Liu JY, Mozafari MS. Agonistul receptorului de hidrocarburi arii, leflunomida, protejează rinichiul ischemic-reperfuzat: rolul Tregs și al celulelor stem. Am J Physiol Regul Integr Comp Physiol. 2012;303:R1136–46.
87. Taki K, Nakamura S, Miglinas M, Enomoto A, Niwa T. Accumulation of indoxyl sulfate in OAT1/3-positive tubular cells in kidneys of patients with chronic renal failure. J Ren Nutr. 2006;16:199–203.
88. Niwa T, Takeda N, Tatematsu A, Maeda K. Acumularea de sulfat de indoxil, un inhibitor al legării medicamentului, în serul uremic, așa cum este demonstrat prin cromatografie lichidă cu fază inversă de suprafață internă. Clin Chem. 1988;34:2264–7.
89. Deguchi T, Nakamura M, Tsutsumi Y, Suenaga A, Otagiri M. Pharmacokinetics and tissue distribution of uraemic indoxyl sulfate in rats. Biopharm Drug Dispos. 2003;24:345–55.
90. Sindhu RK, Vaziri ND. Reglarea citocromului P450 1A2 în insuficiența renală cronică: triptofanul oxidat joacă un rol? Adv Exp Med Biol. 2003;527:401–7.
91. Moriguchi T, Motohashi H, Hosoya T, Nakajima O, Takahashi S, Ohsako S, Aoki Y, Nishimura N, Tohyama C, Fujii-Kuriyama Y, Yamamoto M. Răspuns distinct la dioxină într-un receptor de hidrocarburi arii (AHR)- şoarece umanizat. Proc Natl Acad Sci USA. 2003;100:5652–7.
92. Kim JT, Kim SS, Jun DW, Hwang YH, Park WH, Pak YK, Lee HK. Activitatea de transactivare a receptorului seric de hidrocarburi arii este crescută la pacienții cu diabet de tip 2 cu nefropatie diabetică. J Diabetes Investig. 2013;4:483–91.
93. Lee WJ, Liu SH, Chiang CK, Lin SY, Liang KW, Chen CH, Tien HR, Chen PH, Wu JP, Tsai YC și colab. Deficiența receptorului de hidrocarburi arii atenuează activarea celulelor mezangiale legate de stresul oxidativ și infiltrarea macrofagelor și acumularea de matrice extracelulară în nefropatia diabetică. Semnal antioxid Redox. 2016;24:217–31.
94. Ng HY, Bolati W, Lee CT, Chien YS, Yisireyili M, Saito S, Pei SN, Nishijima F, Niwa T. Indoxyl sulfate downregulates Mas receptor via aril hydrocarbon receptor/nuclear Factor-κB și induce proliferarea celulară și factorul de țesut expresie în celulele musculare netede vasculare. Nefron. 2016;133:205–12.
95. Ng HY, Yisireyili M, Saito S, Lee CT, Adelibieke Y, Nishijima F, Niwa T. Sulfatul de indoxil reduce expresia receptorului Mas prin calea OAT3/ AhR/Stat3 în celulele tubulare proximale. Plus unu. 2014;9:e91517.
96. Yisireyili M, Saito S, Abudureyimu S, Adelibieke Y, Ng HY, Nishijima F, Takeshita K, Murohara T, Niwa T. Activarea indusă de sulfat de indoxil a receptorului (pro)reninului promovează proliferarea celulară și exprimarea factorului tisular în netezirea vasculară celule musculare. Plus unu. 2014;9:e109268.
97. Corre S, Tardif N, Mouchet N, Leclair HM, Boussemart L, Gautron A, Bachelot L, Perrot A, Soshilov A, Rogiers A, et al. Activarea susținută a factorului de transcripție al receptorului de hidrocarburi arii promovează rezistența la inhibitorii BRAF în melanom. Nat Commun. 2018;9:4775.
98. Ishida M, Mikami S, Shinojima T, Kosaka T, Mizuno R, Kikuchi E, Miyajima A, Okada Y, Oya M. Activarea receptorului de hidrocarburi aril promovează invazia carcinomului cu celule renale cu celule clare și este asociată cu prognostic prost și țigară. fum. Int J Cancer. 2015;137:299–310.
99. Chen L, Cao G, Wang M, Feng YL, Chen DQ, Vaziri ND, Zhuang S, Zhao YY. Acidul periodic ZI inhibitor al metaloproteinazei matriceale-13 ameliorează fibroza renală prin atenuarea tranziției epitelial-mezenchimatoase. Mol Nutr Food Res. 2019;63:e1900132.
100. Ishida M, Mikami S, Kikuchi E, Kosaka T, Miyajima A, Nakagawa K, Mukai M, Okada Y, Oya M. Activarea căii receptorului de hidrocarburi arii îmbunătățește invazia celulelor canceroase prin reglarea pozitivă a expresiei MMP și este asociată cu o slabă prognosticul cancerului urotelial al tractului urinar superior. Carcinogeneza. 2010;31:287–95.
101. Suzuki T, Toyohara T, Akiyama Y, Takeuchi Y, Mishima E, Suzuki C, Ito S, Soga T, Abe T. Reglarea transcripțională a polipeptidei care transportă anioni organici SLCO4C1 ca o nouă modalitate terapeutică pentru prevenirea bolii cronice de rinichi. J Pharm Sci. 2011;100:3696–707.
102. Joo MS, Lee CG, Koo JH, Kim SG. miR-125b crescut transcripțional de Nrf2 inhibă represorul AhR, care protejează rinichiul de leziunile induse de cisplatină. Moartea celulară Dis. 2013;4:e899.
103. Zhao YY. Utilizări tradiționale, fitochimie, farmacologie, farmacocinetică și controlul calității Polyporus umbellatus (Pers.) Cartofi prăjiți: o revizuire. J Etnofarmacol. 2013;149:35–48.
104. Tian T, Chen H, Zhao YY. Utilizări tradiționale, fitochimie, farmacologie, toxicologie și control al calității Alisma Orientale (Sam.) Julep: o revizuire. J Etnofarmacol. 2014;158:373–87.
105. Chen H, Tian T, Miao H, Zhao YY. Utilizări tradiționale, fermentație, fotochimie și farmacologia Phellinus linteus o revizuire. Fitoterapia. 2016;113:6–26.
106. Chen DQ, Feng YL, Chen L, Liu JR, Wang M, Vaziri ND, Zhao YY. Acidul portico A îmbunătățește inhibarea melatoninei a tranziției AKI la boala renală cronică prin reglarea axei Gas6/Axl-NF-κB/Nrf2. Free Radic Biol Med. 2019;134:484–97.
107. Wang M, Chen DQ, Chen L, Cao G, Zhao H, Liu D, Vaziri ND, Guo Y, Zhao YY. Inhibitori noi ai componentelor sistemului celular renină-angiotensină, acizii poricoici, țintă fosforilarea Smad3 și calea Wnt/-catenină împotriva fibrozei renale. Br J Pharmacol. 2018;175:2689–708.
108. Gong X, Sucher NJ. Terapia accidentului vascular cerebral în medicina tradițională chineză (TCM): perspective pentru descoperirea și dezvoltarea medicamentelor. Trends Pharma‑col Sci. 1999;20:191–6.
109. Hao H, Zheng X, Wang G. Perspective în descoperirea de medicamente din medicamente naturale folosind farmacocinetica inversă. Trends Pharmacol Sci. 2014;35:168–77.
110. Jiang WY. Înțelepciunea terapeutică în medicina tradițională chineză: o perspectivă din știința modernă. Trends Pharmacol Sci. 2005;26:558–63.
111. Liu X, Wu WY, Jiang BH, Yang M, Guo DA. Instrumente farmacologice pentru dezvoltarea medicinei tradiționale chineze. Trends Pharmacol Sci. 2013;34:620–8.
112. Yang T, Chen YY, Liu JR, Zhao H, Vaziri ND, Guo Y, Zhao YY. Produse naturale împotriva sistemului renină-angiotensină pentru terapia antifibrotică. Eur J Med Chem. 2019;179:623–33.
113. Feng YL, Chen DQ, Vaziri ND, Guo Y, Zhao YY. Inhibitori cu molecule mici ai tranziției epitelial-mezenchimale pentru tratamentul cancerului și fibrozei. Med Res Rev. 2019.
114. Liu D, Chen L, Zhao H, Vaziri ND, Ma SC, Zhao YY. Moleculele mici din produsele naturale vizează calea Wnt/-cateninei ca strategie terapeutică. Biomed Pharmacother. 2019;117:108990.
115. Chen YY, Yu XY, Chen L, Vaziri ND, Ma SC, Zhao YY. Semnalizarea redox în rinichii îmbătrâniți și oportunitate de intervenție terapeutică prin produse naturale. Free Radic Biol Med. 2019;141:141–9.
116. Xue Z, Li D, Yu W, Zhang Q, Hou X, He Y, Kou X. Mecanisme și perspective terapeutice ale polifenolilor ca modulatori ai receptorului de hidrocarburi arii. Funcție alimentară. 2017;8:1414–37.
117. Shinde R, McGaha TL. Receptorul de hidrocarburi arii: conectarea imunității la micromediu. Tendințe Immunol. 2018;39:1005–20.
118. Roman AC, Carvajal-Gonzalez JM, Merino JM, Mulero-Navarro S, Fernandez-Salguero PM. Receptorul arii hidrocarburi în intersecția rețelelor de semnalizare cu valoare terapeutică. Pharmacol Ther. 2018;185:50–63.
119. Kalthof S, Strassburg CP. Contribuția UDP-glucuronic-sialiltransferazelor umane la efectele antioxidante ale propolisului, anghinării și silimarinei. Fitomedicina. 2019;56:35–9.
120. Wattenberg LW, Loub WD. Inhibarea neoplaziei induse de hidrocarburi aromatice policiclice de către indolii naturali. Cancer Res. 1978;38:1410–3.
121. Bjeldanes LF, Kim JY, Grose KR, Bartholomew JC, Bradfeld CA. Agoniști ai receptorilor de răspuns la hidrocarburi aromatice generați din indol- 3-carbinol in vitro și in vivo: comparații cu 2,3,7,8-tetraclorodibenzo-p-dioxină. Proc Natl Acad Sci USA. 1991;88:9543–7.
122. Lamas B, Natividad JM, Sokol H. Receptorul de hidrocarburi arii și imunitatea intestinală. Imunol mucoase. 2018;11:1024–38.
123. Popolo A, Pinto A, Daglia M, Nabavi SF, Farooqi AA, Rastrelli L. Două ținte probabile pentru efectul anticancer al derivaților de indol din legumele crucifere: calea de semnalizare PI3K/Akt/mTOR și receptorul de hidrocarburi arii. Semin Cancer Biol. 2017;46:132–7.
124. Esser C, Rannug A. Receptorul de hidrocarburi arii în fiziologia organelor de barieră, imunologie și toxicologie. Pharmacol Rev. 2015;67:259–79.
125. Sonderby IE, Geu-Flores F, Halkier BA. Biosinteza glucozinolaților – descoperirea genelor și nu numai. Trends Plant Sci. 2010;15:283–90.
126. Mohammadi-Bardbori A, Bengtsson J, Rannug U, Rannug A, Wincent E. Quercetina, resveratrolul și curcumina sunt activatori indirecti ai receptorului de hidrocarburi arii (AHR). Chem Res Toxicol. 2012;25:1878–84.
127. Perez-Jimenez J, Neveu V, Vos F, Scalbert A. Analiza sistematică a conținutului de 502 polifenoli în 452 de alimente și băuturi: o aplicație a bazei de date phenol-explorer. J Agric Food Chim. 2010;58:4959–69.
128. Chen L, Teng H, Xie Z, Cao H, Cheang WS, Skalicka-Wozniak K, Georgiev MI, Xiao J. Modificări ale flavonoidelor dietetice spre bio-activitate îmbunătățită: o actualizare a relației structură-activitate. Crit Rev Food Sci Nutr. 2018;58:513–27.
129. Jin UH, Park H, Li X, Davidson LA, Allred C, Patil B, Jayaprakasha G, Orr AA, Mao L, Chapkin RS și colab. Modularea dependentă de structură a activităților mediate de receptorul de hidrocarburi arii de către flavonoide. Toxicol Sci. 2018;164:205–17. 130. Yang T, Feng YL, Chen L, Vaziri ND, Zhao YY. Flavonoidele naturale dietetice tratează cancerul prin țintirea receptorilor de hidrocarburi arii. Crit Rev Toxicol. 2019.
131. Androutsopoulos VP, Papakyriakou A, Vourloumis D, Tsatsakis AM, Spandidos DA. Flavonoide dietetice în terapia și prevenirea cancerului: substraturi și inhibitori ai enzimelor CYP1 citocromului P450. Farmacia Ther. 2010;126:9–20.
132. Chen AY, Chen YC. O revizuire a flavonoidului dietetic, kaempferol, asupra sănătății umane și a chimioprevenției cancerului. Food Chim. 2013;138:2099–107.
133. Zhao YY, Wang HL, Cheng XL, Wei F, Bai X, Lin RC, Vaziri ND. Analiza metabolomică dezvăluie asocierea dintre anomaliile lipidelor și stresul oxidativ, inflamație, fibroză și disfuncția Nrf2 în nefropatia indusă de acid aristolohic. Sci Rep. 2015;5:12936.
134. Debelle FD, Vanherweghem JL, Nortier JL. Nefropatia cu acid aristolohic: o problemă la nivel mondial. Rinichi Int. 2008;74:158–69.
135. Michl J, Ingrouille MJ, Simmonds MS, Heinrich M. Analogi ai acidului aristolohic natural și toxicitatea acestora. Nat Prod Rep. 2014;31:676–93.
136. Chan CK, Liu Y, Pavlovic NM, Chan W. Etiology of Balkan endemic nephropathy: an update on aristolochic acids expunere mecanismes. Chem Res Toxicol. 2018;31:1109–10.
137. Wang K, Feng C, Li C, Yao J, Xie X, Gong L, Luan Y, Xing G, Zhu X, Qi X, Ren J. Baicalin protejează șoarecii de leziunea renală indusă de acid aristolohic I prin inducerea CYP1A prin receptorul hidrocarburilor aromatice. Int J Mol Sci. 2015;16:16454–68.
138. Feng C, Xie X, Wu M, Li C, Gao M, Liu M, Qi X, Ren J. Tanshinone I protejează șoarecii de leziunea renală indusă de acid aristolohic I prin inducerea CYP1A. Environ Toxicol Pharmacol. 2013;36:850–7.
139. Zhao YY, Lin RC. Metabolomica în nefrotoxicitate. Adv Clin Chem. 2014;65:69–89.
140. Zhao YY, Vaziri ND, Lin RC. Lipidomica: o nouă perspectivă asupra bolilor de rinichi. Adv Clin Chem. 2015;68:153–75.
141. Hocher B, Adamski J. Metabolomics pentru utilizare clinică și cercetare în boala cronică de rinichi. Nat Rev Nephrol. 2017;13:269–84.
142. Zhao YY, Liu J, Cheng XL, Bai X, Lin RC. Studiu de metabonomie urinară asupra modificărilor biochimice într-un model experimental de insuficiență renală cronică de către adenină pe baza UPLC Q-TOF/MS. Clin Chim Acta. 2012;413:642–9.
143. Zhang ZH, Chen H, Vaziri ND, Mao JR, Zhang L, Bai X, Zhao YY. Semnături metabolomice ale bolii cronice de rinichi de diverse etiologii la șobolani și oameni. J Proteome Res. 2016;15:3802–12.
144. Chen DQ, Feng YL, Cao G, Zhao YY. Produsele naturale ca sursă de terapie antifibrotică. Trends Pharmacol Sci. 2018;39:937–52.
145. Moloney MG. Produse naturale ca sursă pentru noi antibiotice. Trends Pharmacol Sci. 2016;37:689–701.
146. Newman DJ, Cragg GM. Produsele naturale ca surse de noi medicamente din 1981 până în 2014. J Nat Prod. 2016;79:629–61.
147. Rodrigues T, Reker D, Schneider P, Schneider G. Counting on natural products for drug design. Nat Chem. 2016;8:531–41.
148. Harvey AL, Edrada-Ebel R, Quinn RJ. Reapariția produselor naturale pentru descoperirea medicamentelor în epoca genomicii. Nat Rev Drug Discov. 2015;14:111–29.
149. Butler MS, Robertson AA, Cooper MA. Produs natural și medicamente derivate din produse naturale în studiile clinice. Nat Prod Rep. 2014;31:1612–61.
150. Xiao J. Agliconii flavonoide dietetice și glicozidele lor: care prezintă o semnificație biologică mai bună? Crit Rev Food Sci Nutr. 2017;57:1874–905.
151. Edeling M, Ragi G, Huang S, Pavenstadt H, Susztak K. Căile de semnalizare de dezvoltare în fibroza renală: rolurile Notch, Wnt și Hedgehog. Nat Rev Nephrol. 2016;12:426–39.
152. Chen L, Yang T, Lu DW, Zhao H, Feng YL, Chen H, Chen DQ, Vaziri ND, Zhao YY. Rolul central al dereglării TGF-/Smad în progresia bolii renale cronice și potențialele ținte ale tratamentului acesteia. Biomed Pharmacother.
2018;101:670–81.
