Efectul încărcării nutriționale cu calciu și fosfat asupra cineticii particulelor de calciproteine la adulții cu funcție renală normală și afectată
Jul 25, 2023
Abstract
Plasma se apropie de metastabilitatea în ceea ce privește conținutul său de calciu și fosfat, cu doar perturbări minore ale activității ionice necesare pentru a susține creșterea cristalelor odată nucleate. Fiziologic, calciul și fosfatul sunt absorbite intermitent din dietă în fiecare zi, totuși concentrațiile plasmatice ale acestor ioni deviază minim post-prandial. Aceasta implică existența unui sistem-tampon de minerale din sânge pentru a sechestra fosfații de calciu și a minimiza riscul de depunere în țesuturile moi. Particulele de calciproteină (CPP), coloizii minerali-proteici endogeni care conțin proteina plasmatică fetuina-A, pot îndeplini această funcție, dar lipsesc dovezi definitive care să lege încărcarea minerală alimentară cu formarea lor. Aici demonstrăm că CPP se formează ca răspuns fiziologic normal la hrănire la adulții sănătoși și că acest lucru are loc în ciuda modificării minime a markerilor minerali convenționali din ser. În plus, la persoanele cu boală cronică de rinichi (CKD), la care manipularea mineralelor este afectată, arătăm că atât nivelurile de post, cât și cele postprandiale ale precursorilor CPP sunt semnificativ crescute și puternic corelate invers cu funcția rinichilor. Acest studiu evidențiază contribuția importantă, dar adesea neglijată, a biochimiei coloidale la homeostazia minerală și oferă o nouă perspectivă asupra dereglării metabolismului mineral în CKD.

Click aici pentru a cumpara produsele Cistanche
Introducere
Calciul și fosfatul formează săruri foarte insolubile în soluție apoasă și, în timp ce metabolismul în toate organismele vii este dependent de acești nutrienți esențiali, coexistența lor în fluidele biologice creează un risc inerent de mineralizare și necesitatea unei reglementări stricte1. Majoritatea fluidelor extracelulare, cum ar fi plasma, sunt considerate metastabile sau se apropie de metastabilitatea în ceea ce privește activitățile ionice de calciu și fosfat2, susținând ușor creșterea cristalelor dacă sunt nucleate. Această tendință de precipitare a calciului și a fosfatului a fost valorificată de vertebrate pentru proprietățile lor biomecanice unice în timpul evoluției țesuturilor scheletice și dentare. Totuși, în același timp, aceasta a impus mecanisme de mobilizare rapidă și transport eficient în vrac al precursorilor minerali pentru a satisface cerințele de creștere și reparare a acestor țesuturi dure, precum și strategii de restricționare a mineralizării la aceste locuri și prevenirea calcificării nedorite în țesuturile moi3. . Într-adevăr, chiar și creșterile modeste ale concentrațiilor plasmatice de calciu și fosfat sunt asociate cu un risc crescut de calcificare patologică a arterelor și țesuturilor4. Deoarece excesul de calciu și fosfat sunt excretați aproape exclusiv de rinichi, acest risc, împreună cu sechelele cardiovasculare asociate, este substanțial mai mare la cei cu boală renală cronică (IRC), unde tulburările metabolismului mineral devin evidente cu scăderi relativ mici ale filtrării glomerulare. rata (GFR)5,6. Având în vedere abundența de calciu și fosfat din dieta la care mamiferele sunt expuse intermitent, s-ar putea bănui că riscul de mineralizare ectopică este cel mai mare după o masă din cauza creșterii anticipate a ionilor minerali absorbiți din intestin. Totuși, contrar acestei așteptări, concentrațiile plasmatice de calciu și fosfat se modifică minim în perioada postprandială și, în timp ce excreția urinară crescută ajută la menținerea homeostaziei7, acest răspuns nu este instantaneu și întârzie cu câteva ore după ingestia de cantități milimolare de calciu și fosfat8. Ca o soluție la această provocare fiziologică, a fost suspectat de multă vreme un sistem prin sânge pentru tamponarea și transportul mineralelor9, iar atenția recentă s-a îndreptat către complexele minerale-proteine coloidale care ar putea îndeplini această funcție și ar putea însoți în siguranță fuxul intermitent de minerale prin extracelular. fluid către locurile de utilizare sau eliminare10.
În plasmă, cel mai puternic și abundent regulator al mineralizării proteinelor este glicoproteina fetuin-A11 derivată din ficat, care interacționează cu complexe minerale-proteine coloidale în curs de dezvoltare pentru a forma particule de calciproteină (CPP)12,13. În mod similar modului în care apolipoproteinele își solubilizează încărcătura lipidică pentru transport, fetuinA stabilizează fosfații de calciu slab solubili, prevenind creșterea și precipitarea cristalelor, facilitând în același timp absorbția lor în țesuturi pentru utilizare sau eliminare14-16. O incapacitate de a produce sau de a stabiliza suficient CPP, așa cum se observă la șoarecii knockout fetuin-A, are ca rezultat unul dintre cele mai severe fenotipuri de calcifiere ectopică cunoscute17, în care complexele care conțin minerale precipită direct în lumenul microvasculaturii ducând la ocluzie, ischemie, necroză și fbroză18. CPP este generată printr-o serie de etape ordonate, inițial cu legarea unor clustere formate spontan de ioni de calciu și fosfat la fetuina-A, formând monomeri calciproteici (CPM)19, care servesc apoi drept blocuri de construcție pentru structurile polimerice mai mari; în primul rând, coalescerea pentru a forma CPP primar sferic (CPP-I) care conține fosfat de calciu amorf, înainte de a se transforma în CPP secundar elipsoidal mai mare și mai dens (CPP-II) care conține hidroxiapatită cristalină12.
Dincolo de presupusul rol fiziologic al formării CPP în sechestrarea și dispersarea excesului de minerale, niveluri crescute sunt observate și în stările de metabolism mineral afectat, inclusiv în CKD20. În acest context, nivelurile serice mai ridicate de CPM și CPP au fost legate de un risc crescut de evenimente cardiovasculare21–25 și de mortalitate22. Studiile preclinice sugerează că CPP poate induce direct calcificarea celulelor musculare netede vasculare26,27, activarea căilor celulare inflamatorii și citotoxice28,29, precum și leziuni vasculare luminale și endoteliale30. Luate împreună, s-a propus că expunerea prelungită la niveluri cronice crescute de CPP seric poate ajuta la explicarea legăturilor dintre excesul de minerale din dietă și rezultatele slabe ale pacientului în CKD14,31. În mod intrigant, datele recente sugerează, de asemenea, că CPM circulant este filtrat la glomerul29, ceea ce implică faptul că insuficiența renală poate afecta metabolismul CPP prin mecanisme multiple.
Progresele metodologice recente permit cuantificarea directă a CPM32, CPP-I și CPP-II33, aceste teste fiind acum aplicate în mai multe studii clinice observaționale și intervenționale24,25,34–39. O altă metodă complementară nouă pentru evaluarea acestui sistem este testul T50, o evaluare funcțională a capacității serului de a rezista la formarea ex vivo a CPP-II atunci când este provocat cu cantități suprasaturate de calciu și fosfat40. Un T50 mai scăzut a fost asociat în mod constant cu un risc crescut de patologie vasculară și mortalitate la indivizii cu funcție renală normală41, precum și în diferite cohorte de CKD, incluzând atât CKD fără dializă22,42,43, cât și CKD dependentă de dializă44. În plus față de cinetica formării CPP-II, dimensiunea (raza hidrodinamică) a moleculelor CPP-II generate în testul T50 poate fi, de asemenea, măsurată40,45 și poate oferi informații prognostice suplimentare despre riscul vascular46,47.
Noțiunea de origine alimentară a CPP este puternic susținută de observația că hrănirea bogată în fosfat este asociată cu niveluri ambientale crescute de CPM48 și CPP33 în studiile pe animale și reducerea CPM34 și CPP37 serice la pacienții hemodializați tratați cu lianți intestinali de fosfat. Cu toate acestea, lipsește observarea definitivă a efectului aportului de minerale nutriționale asupra cineticii acute a CPP la oameni. În plus, impactul CKD asupra metabolismului CPP post-prandial nu a fost încă documentat. Pentru a aborda aceste lacune cheie de dovezi, am efectuat un studiu controlat al efectului aportului alimentar standardizat asupra mărimii CPM, CPP-I, CPP-II, T50 și CPP-II serice, la adulți aflați în post cu funcție renală normală sau afectată.

Extract de Cistanche
Metodologie
1. Populația de studiu.
Am studiat 14 indivizi cu CKD și 16 martori sănătoși de vârstă și sex. Fiecare participant trebuia să aibă cel puțin 18 ani pentru a fi eligibil. Participanții au fost excluși dacă: (i) au avut antecedente de boli minerale sau osoase, altele decât cele legate de CKD; (ii) au fost tratați cu un liant intestinal de fosfat sau calcitriol; sau (iii) au avut o tulburare gastrointestinală, antecedente de intoleranță la lactoză sau nu au fost dispuși să consume masa de studiu. Pentru grupul CKD, am recrutat șapte indivizi cu o rată estimată de filtrare glomerulară (eGFR) între 30 și 60 mL/min/1,73 m2 și șapte cu eGFR.<30 mL/min/1.73 m2, excluding participants who required dialysis or with a previous kidney transplant. Healthy controls had no history of chronic medical conditions and had normal kidney function (eGFR>60 ml/min/1,73 m2). Studiul a fost realizat prin Declarația de la Helsinki.
Toate persoanele au furnizat consimțământul informat în scris, iar studiul a fost aprobat de comitetul local de etică (Melbourne Health Human Research Ethics Committee MH2018.363).
2. Procedura.
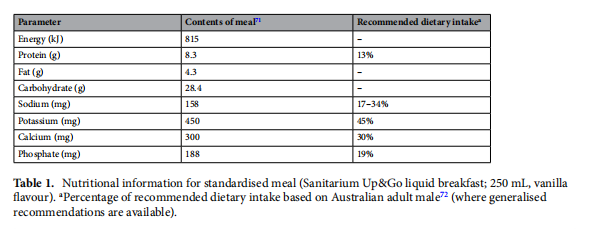
Fiecare participant a fost studiat după un post peste noapte, iar recoltarea de probe a început între 7.30 și 9.30 dimineața. La începutul perioadei de studiu a fost introdusă o canulă intravenoasă. Înainte ca fiecare probă de sânge să fie colectată, o extragere inițială de 5 ml din canulă a fost aruncată. Două probe inițiale de sânge a jeun au fost prelevate la 30 de minute una de cealaltă pentru a ține cont de variația inițială. Valorile medii ale acestor două puncte de timp au fost folosite ca „timp 0”. Imediat după colectarea celei de-a doua probe de post, participanții au consumat o masă standardizată (mic dejun lichid Sanitarium Up&Go; 250 ml, aromă de vanilie) care conținea 815 kJ energie, 300 mg calciu și 188 mg fosfat (Tabelul 1). Participanții au fost instruiți să consume întreaga băutură în 5 minute. Probele de sânge în serie au fost colectate la cinci momente postprandiale (30, 60, 120, 180 și 240 min) de la începutul mesei. În timpul perioadei de studiu, participanților li s-a permis să bea apă, dar nu li sa permis să consume alte alimente sau băuturi.
3. Măsuri de rezultat.
S-a recoltat sânge pentru măsurarea repetată a markerilor noi ai metabolismului mineral (CPM, CPP-I, CPP-II, T50 și dimensiunea CPP-II) la fiecare punct de timp. Fetuina-A a fost măsurată în fiecare moment, având în vedere rolul său ca principală proteină de legare a mineralelor prezentă în CPM și CPP. Am măsurat, de asemenea, fosfatul seric, calciul total, magneziul, albumina și bicarbonatul la fiecare moment și hormonul paratiroidian intact (PTH) și factorul de creștere a fibroblastelor intact-23 (iFGF23) la trei momente ({{12) }}, 120 și 240 min). Citratul seric a fost măsurat la 0, 30 și 60 de minute. Ureea serică, creatinina și 1,25 dihidroxi vitamina D au fost măsurate o dată la momentul inițial a jeun (0 min). Probele de sânge pentru noi markeri ai metabolismului mineral, PTH, iFGF23, 1,25 dihidroxi vitamina D și citrat seric, au fost lăsate să se coaguleze timp de 30 de minute înainte de centrifugare, iar apoi alicote de ser au fost depozitate la -80 de grade până la analiza lotului. Toate celelalte măsurători biochimice au fost efectuate în momentul recoltării probei folosind metode standard de laborator.
4. Teste de filtrare cu gel și citometrie pentru CPM și CPP.
Am folosit două teste complementare pentru a cuantifica fracții diferite ale pool-ului de CPP circulant49. Ambele teste folosesc derivatul de bifosfonat marcat fluorescent, OsteoSense 680EX (Perkin Elmer), care se leagă în mod specific la fosfatul de calciu în fază solidă și preferabil la fazele cristaline (de exemplu, hidroxiapatita). Metoda „gel-flatrare” a lui Miura et al.32 a fost folosită pentru a măsura mici (<50 nm diameter), low-density mineral-laden fetuin-A colloids. Briefly, frozen serum samples were thawed for 24 h at 25 °C to induce aggregation of CPM and phase transition to crystalline calcium phosphate. Samples were then centrifuged for 30,000g for 2 h at 4 °C to remove larger CPP-I and CPP-II, leaving less dense crystal-laden fetuin-A monomer and multimers for staining with OsteoSense (0.5 µM) in HEPES-buffered DMEM (pH 8.0). Unbound dye was subsequently removed by gel filtration (Micro Bio-Spin® Columns with Bio-Gel® P-30, Bio-Rad) and the resultant fluorescence was measured using an infrared scanner (Odyssey CLx, LI-COR; EX 685 nm, EM 700 nm). Miura and colleagues32 referred to the mineral detected as low-density (L)-CPP, however, here we refer to them as CPM to reflect the origin of this mineral fraction in vivo. In our hands, the mean interassay analytical coefficient of variation (CVA) for the CPM assay was 4.9%.
Pentru analiza citometrică în flux, alicote de ser congelat au fost procesate folosind procedurile standardizate descrise anterior50. CPP-I și CPP-II au fost măsurate așa cum s-a descris anterior, folosind o configurație de citometru de flux BD FACSVerse pentru a rezolva particulele<200 nm from the background and operate with fluorescence triggering on OsteoSense-positive events33,37. In this assay, CPP is distinguished from membrane-delimited mineral-containing extracellular vesicles using phosphatidyl serine–binding cadherin-FITC (Haematologic Technologies Inc., Essex Junction, VT). CPP-I and CPP-II were distinguished by differences in side scatter (SSC) intensity (related to particle size) and OsteoSense fluorescence intensity. Interassay CVA for CPP-I and CPP-II were<15% and<10%, respectively.
5. Alți markeri minerali.
Serul T50 a fost măsurat de Calciscon AG, Biel, Elveția, așa cum s-a descris anterior folosind un nefelometru Nephelostar (BMG Labtech, Ortenberg, Germania)40. Valoarea medie a CVA intertest pentru T50 a fost de 3,4 %. Raza hidrodinamică CPP-II a fost măsurată prin împrăștierea dinamică a luminii folosind un cititor de plăci DynaPro II (Wyatt Technology, Santa Barbara, CA, SUA) așa cum este descris de Chen și colab.47. Tea CVA intertest pentru dimensiunea CPP-II a fost de 4%. Testele imunologice comerciale au fost utilizate pentru a măsura iFGF23 (Kainos Laboratories, Tokyo, Japonia), 1,25 dihidroxi vitamina D Immunodiagnostic Systems, Boldon, Marea Britanie) și fetuin-A (R&D Systems, Minneapolis, SUA) conform instrucțiunilor producătorului. Media CVA intertestare a fost de 3,8 la sută, 5,5 la sută și, respectiv, 3,2 la sută. Citratul seric a fost măsurat utilizând un test colorimetric (Sigma-Aldrich, Darmstadt, Germania) cu un CVA intertest mediu de 3,5%.
6. Analiză statistică.
Using GLIMPSE, a validated linear mixed model power and sample size calculator51, we estimated that 10 participants would provide>Putere de 90 procente pentru a detecta o dublare a CPP în perioada postprandială cu o rată de eroare de tip I de 0,05. Studiul nu a fost alimentat pentru a detecta o diferență între grupuri.
Datele demografice și biochimice de post au fost comparate între grupuri folosind un test t neîmperecheat sau testul Kruskal-Wallis pentru variabilele normale și, respectiv, înclinate, și un test chi-pătrat pentru variabilele categorice.
Ne-am propus să descriem răspunsul postprandial în interiorul și între grup pentru fiecare parametru repetat. Pentru a face acest lucru, am adaptat modele liniare cu efecte mixte (LMM) pentru fiecare parametru, utilizând o abordare de probabilitate maximă restrânsă și cu o matrice de covarianță nestructurată52. Pentru fiecare LMM am modelat grup, timpul categoric și interacțiunea grup-cu-timp ca efecte fixe și a fost inclusă o interceptare aleatorie pentru fiecare participant pentru a ține seama de corelarea măsurilor repetate. Grupul de control și timpul „0” au fost utilizate ca valori de referință pentru grup și, respectiv, timp. Estimările coeficienților pentru termenii de interacțiune grup-de-timp au fost utilizate pentru a testa diferențele în răspunsul post-prandial între grupurile CKD și de control. După ajustarea fiecărui LMM, am efectuat, de asemenea, comparații post-hoc în perechi pentru a testa diferențele dintre valorile medii între grupuri la fiecare punct de timp și pentru a testa abaterea de la linia de bază de post în cadrul fiecărui grup. Pentru aceste comparații în perechi, am folosit metoda de corecție Bonferroni pentru a ajusta pentru comparații multiple. Dimensiunea CPM, CPP-I, CPP-II, CPP-II, PTH și iFGF23 au fost transformate în mod natural înainte de montarea LMM-urilor pentru a asigura distribuția normală a reziduurilor. Pentru ușurința interpretării, estimările coeficienților pentru termenii de interacțiune din aceste modele au fost apoi exponențiate pentru a obține estimări ale modificării procentuale. Pentru LMM-ul CPM, termenii de interacțiune grup cu timp au sugerat o diferență semnificativă în răspunsul post-prandial între grupuri. Pentru a explora în continuare efectul funcției renale asupra nivelurilor post-prandiale ale CPM, am calculat, de asemenea, aria de sub curbă (AUC) pentru CPM utilizând metoda spline cubice (timp 0 până la 240 min) și am examinat relația dintre eGFR , AUC și concentrația maximă de CPM (folosind corelația rangului Spearman), precum și între CKD și timpul de concentrație maximă de CPM (folosind testul chi-pătrat).
Mai multe probe au avut niveluri nedetectabile de CPP-I (2 probe în grupul martor și 6 în grupul CKD) sau CPP-II (5 în grupul de control și 10 în grupul CKD). Pentru analizele principale, a fost utilizată limita inferioară de cuantificare pentru test (133 particule/mL) pentru aceste valori cenzurate în stânga. Pentru a evalua prejudecățile potențiale din această abordare, am efectuat o analiză de sensibilitate în care LMM-urile pentru CPP-I și CPP-II au fost readaptate după imputarea valorilor cenzurate cu stânga folosind regresia Tobit pe mai multe niveluri, în care timpul și grupul au fost introduse ca variabile independente 53.
Valori p cu două cozi<0.05 were considered significant. All data were analyzed using Stata MP version 17.0 (StataCorp, College Station, USA) and figures were produced using GraphPad Prism version 9.2.0 (GraphPad Sofware, San Diego, USA).

Herba Cistanche
Discuţie
Din câte cunoștințele noastre, acesta este primul studiu care raportează un efect postprandial semnificativ al aportului nutrițional asupra nivelurilor serice de CPM, CPP-I și CPP-II la oameni. Aceste efecte au fost comune persoanelor cu funcție renală normală și afectată; cu toate acestea, excursia post-prandială a CPM seric a fost mult mai pronunțată la participanții CKD. De asemenea, am găsit un efect postprandial precoce și tranzitoriu asupra T50, care a fost prezent indiferent de funcția rinichilor și însoțit de o creștere concomitentă a fetuinei-A serice.
Descoperirile noastre sunt în concordanță cu ideea că absorbția intestinală a unei încărcături minerale dietetice poate duce direct la formarea CPM, CPP-I și CPP-II circulante. Acest lucru a fost propus anterior10,15,16, dar se bazează în mare parte pe date despre animale33,48. În schimb, dovezile la oameni au fost indirecte, provenind din studiile de lianți intestinali de fosfat la pacienții cu CKD dependenți de hemodializă34,37,55. Un mic studiu realizat de Yamada et al. a sugerat o variație diurnă a CPP seric cu vârfuri post-prandiale, cu toate acestea, acest studiu a folosit o tehnică de analiză mai veche care nu a putut cuantifica separat CPM și subspeciile CPP, iar participanții au fost cu toții spitalizați pentru gestionarea diabetului instabil56. În schimb, toți participanții la acest studiu au fost stabili din punct de vedere clinic și, din câte știm, pentru prima dată, am demonstrat că excursiile post-prandiale sunt observate nu numai la indivizii cu BRC, ci și la adulții sănătoși, dovedind rolul. a formării CPM și CPP în răspunsul fiziologic normal la ingestia de alimente.
Creșterile serice ale CPM și CPP au fost observate chiar și după încărcături minerale nutriționale relativ modeste și relevante din punct de vedere fiziologic (Tabelul 1). În schimb, a existat o variație minimă post-prandială în markerii mai convenționali ai metabolismului mineral. Studiile anterioare au arătat, în mod similar, o abatere postprandială limitată a fosfatului7,57, cu excepția cazului în care subiecții sunt provocați cu încărcături farmacologice mari58,59. În sănătate, fosfatul total din organism este reglat, astfel încât absorbția intestinală netă este egalată cu excreția urinară8. Cu toate acestea, acest răspuns nu este instantaneu și poate fi observată o întârziere de câteva ore înainte de a avea loc creșterea excreției urinare de fosfat, chiar și atunci când încărcătura de fosfat este administrată intravenos8. În schimb, modelele animale au demonstrat că alte mecanisme, non-renale, servesc la menținerea concentrațiilor ionice serice mai acut, prin distribuție către oase și alte țesuturi59-61. Este plauzibil că formarea CPM și CPP poate fi un important depozit temporar suplimentar de fosfat (și calciu), care poate tampona în mod acut încărcăturile minerale locale, cum ar fi cele din sistemul gastrointestinal14. Proprietățile fizico-chimice ale CPM și CPP înseamnă că pot exista cantități mari de minerale altfel insolubile în circulație fără risc de precipitare, ceea ce facilitează în mod aparent transportarea în siguranță a mineralelor în vrac către locurile de utilizare sau eliminare.
Am observat o creștere tranzitorie a fetuinei-A serice în grupul CKD. În schimb, fetuina-A a părut stabilă la controale, totuși, când comparațiile în perechi au fost repetate fără corecție pentru comparații multiple, au existat creșteri semnificative la 30 și 60 de minute la controale (Tabelul suplimentar S8), ceea ce indică faptul că este posibil să fi fost insuficientă pentru a detecta un efect de bază. Dincolo de a fi un reactant negativ de fază acută, cu niveluri puternic suprimate ca răspuns la infamarea acută și cronică62, se știe puțin despre alte mecanisme care reglează direct sinteza hepatică și secreția fetuinei-A și există puține date anterioare despre diurne, sau variaţie acută post-prandială la orice specie. Având în vedere creșterea observată a fetuinei-A serice după hrănire, în special în grupul CKD, și rolul necesar al fetuinei-A în formarea CPM și CPP, este intrigant să ne gândim dacă hrănirea poate fi „sesizată” printr-un mecanism încă necunoscut, ducând la eliberarea hepatică a fetuinei A să coincidă cu un aflux de minerale din intestine. Într-adevăr, Uedono și colab. a sugerat recent că CPP în sine poate fi un declanșator al expresiei fetuinei-A în hepatocitele cultivate63. Astfel, mecanismele care controlează eliberarea fetuinei-A și răspunsul lor la încărcarea minerală justifică investigații suplimentare.
T50 este o evaluare funcțională a capacității serului de a rezista ex vivo la formarea CPP-II, reprezentând un compozit de diverși factori de potențare (inclusiv calciu și fosfat) și inhibare (inclusiv fetuină-A, albumină, magneziu, citrat și bicarbonat)40. Am observat o creștere precoce, dar tranzitorie, a T50. Acest lucru a fost observat în ambele grupuri, dar în grupul CKD, vârful a fost coincident cu creșteri ale fetuinei-A serice. În plus, printre toți participanții, modificarea T50 față de valoarea inițială a fost foarte strâns corelată cu modificarea fetuinei-A serice (Fig. S2 suplimentară), sugerând că fetuina-A poate fi principalul factor care stă la baza modificărilor observate în T50. Într-adevăr, nu am găsit modificări corespunzătoare postprandiale timpurii la alți modulatori cunoscuți ai T50 (fosfat seric, calciu, bicarbonat, magneziu sau albumină), deși acest lucru nu exclude modificări mai subtile ale unuia sau unei combinații dintre acești factori. . De exemplu, a fost prezentă o interacțiune pozitivă grup cu timp pentru bicarbonatul seric în grupul CKD la 120 de minute, care s-a suprapus cu creșterea T50. În ceea ce privește fetuina-A, a existat, de asemenea, o corelație între modificarea bicarbonatului și a T50 față de valoarea inițială (Fig. S4 suplimentară), deși aceasta a fost relativ slabă în comparație cu corelația cu primul (r=0.385 vs. r=0.839). Cu toate acestea, „mareea alcalină” post-prandială este un fenomen recunoscut și este plauzibil că mai mulți factori au contribuit la modificările post-prandiale observate în T5064. Masa de studiu conținea, de asemenea, o cantitate surprinzătoare de citrat (~16 mM), un inhibitor puternic cunoscut al formării CPP, totuși, deși a existat o mică creștere a citratului seric în grupul CKD, această schimbare nu a coincis cu modificările observate în T50 și nici nu a existat nicio corelație generală între modificarea T50 și citratul seric în ambele grupuri. Alți modulatori ai T50 descriși anterior, cum ar fi pirofosfatul și zincul, nu au fost măsurați în acest studiu. Deși acești factori, sau alți încă necunoscuți, ar fi putut, de asemenea, să fi contribuit la creșterea observată post-prandială a T50, observăm că sunt în general necesare schimbări destul de substanțiale ale concentrației acestor molecule anorganice mici pentru a avea un impact semnificativ asupra T5065. Spre deosebire de efectele post-prandiale asupra T50, raza hidrodinamică a CPP-II a rămas aparent neschimbată în ambele grupuri.

Cistanche capsule
În timp ce s-au observat excursii post-prandiale ale CPM în ambele grupuri, nivelurile CPM au fost în mod constant mai mari în grupul CKD la fiecare dintre momentele de timp, iar termenii de interacțiune grup-cu-timp au indicat că amploarea răspunsului post-prandial a fost semnificativ mai mare. la participanții CKD decât la martori. În consecință, în analiza exploratorie, a existat o corelație puternică între eGFR și ASC CPM și concentrația maximă. Nivelurile maxime de CPM au avut, de asemenea, tendința să apară mai târziu în grupul CKD. Teoretic, aceste diferențe ar putea indica o producție crescută de CPM în urma aportului nutrițional și/sau o capacitate afectată de a elimina CPM la cei cu CKD. Acesta din urmă este susținut de date recente ale lui Koeppert și colab., care au folosit microscopia cu doi fotoni vii pentru a arăta că CPM circulant este în mod predominant eliminat prin filtrare glomerulară la șoareci29. Prin urmare, o predicție rezonabilă poate fi că capacitatea de a elimina CPM devine afectată pe măsură ce GFR scade. Cu toate acestea, modificări ale altor aspecte ale homeostaziei minerale, inclusiv turnover-ul osos66 și excreția renală întârziată a încărcăturilor acute de fosfat7,59 sunt, de asemenea, observate frecvent în CKD și ar putea foarte bine să fi contribuit la creșteri ale nivelurilor postprandiale. Dovezile recente au pus sub semnul întrebării ideea de mult timp potrivit căreia CKD afectează absorbția netă a fosfatului intestinal57,67,68. Cu toate acestea, am observat că șase dintre cei 14 indivizi din grupul CKD luau colecalciferol. Având în vedere potențialul efectelor stimulatoare ale vitaminei D asupra absorbției minerale intestinale, am efectuat o analiză exploratorie ad-hoc pentru a testa dacă utilizarea vitaminei D nutriționale a afectat răspunsul acut al CPM, CPP-I și CPP-II la hrănire (Tabelele suplimentare S9–S11). În afară de o singură interacțiune pozitivă grup-cu-timp pentru CPP-I la 30 de minute la cei care au luat colecalciferol, toți ceilalți termeni de interacțiune și comparațiile post-hoc perechi pentru CPM, CPP-I și CPP-II nu au fost semnificative, sugerând că colecalciferol Este puțin probabil ca utilizarea să fi avut un efect substanțial asupra cineticii CPM/CPP postprandiale. În timp ce dimensiunea mică a eșantionului și potențialul de confuzie pot împiedica concluziile definitive, lipsa efectului poate reflecta, de asemenea, predominanța absorbției fosfatului prin calea paracelulară atunci când mineralul este abundent, care nu este reglat activ de axa vitaminei D69.
Spre deosebire de CPM, nu am observat un efect puternic asupra funcției renale nici în CPP-I, nici în CPP-II. Spre deosebire de CPM, CPP circulant este în primul rând eliminat din circulație prin mecanisme non-renale. Modelele animale și in vitro au sugerat eliminarea rapidă a CPP-I predominant de către celulele endoteliale sinusoidale hepatice28 și a CPP-II de către macrofagele rezidente ale ficatului și splinei70. Este plauzibil că, în timp ce participanții din grupul nostru cu CKD au prezentat dovezi ale metabolismului CPM alterat, că aceste căi discrete de eliminare a CPP au fost suficiente pentru a menține profilurile CPP postprandiale normale. Am anticipat că grupul cu BRC ar avea niveluri clar mai mari de CPP în comparație cu controalele bazate pe studii anterioare, deși aceste studii au înrolat pacienți cu BRC mai avansate care erau dependenți de dializă33 sau au folosit metoda mai veche și indirectă de măsurare a CPP20,23. Persoanele cu BRC mai avansată decât cele studiate aici pot prezenta diferențe mai mari în nivelurile CPP postprandiale și postprandiale. Lipsa de separare pentru CPP între CKD și grupul nostru de control se poate datora și numărului nostru limitat de participanți, care ne-a limitat, de asemenea, capacitatea de a testa în mod oficial un efect al stadiului CKD (Fig. S6 suplimentară). Într-adevăr, studiul nostru s-a bazat pe examinarea răspunsurilor post-prandiale, mai degrabă decât a diferențelor între grupuri. De remarcat, CPP-I a părut să revină la nivelurile de post mai devreme la controlul față de participanții cu CKD și a existat o interacțiune pozitivă de la grup la timp pentru CPP-II la participanții cu CKD la 120 de minute. Ambele descoperiri semnalează potențial că este posibil să fi observat efecte mai pronunțate între grupuri într-o cohortă mai mare. Imprecizie analitică mai mare pentru măsurătorile CPP bazate pe citometrie de flux ar putea să fi contribuit, de asemenea, la constatările nule.
Pe lângă faptul că oferă noi perspective asupra fiziologiei metabolismului CPM și CPP, studiul nostru are, de asemenea, relevanță directă pentru optimizarea utilizării acestor noi markeri ai metabolismului mineral în studiile viitoare. În timp ce fiecare dintre aceste teste noi s-a arătat promițătoare în munca clinică timpurie, foarte puține studii au raportat43 sau au controlat starea de post/absorbție46,56. În acest studiu, mai multe persoane au avut niveluri nedetectabile de CPP-I sau CPP-II în perioada de post și timpurie postprandială, iar acest efect profund al postului asupra CPP seric este în sine o finanțare neraportată anterior și notabilă. În schimb, nivelurile CPM de jeun au fost măsurabile și semnificativ mai mari în grupul CKD decât în grupul de control, ceea ce sugerează că creșterile susținute ale CPM s-ar putea să nu se manifeste neapărat în niveluri crescute ale CPP la cei cu CKD nedependentă de dializă.
Studiile epidemiologice anterioare au sugerat legături între nivelurile crescute de CPM și CPP cu o serie de markeri surogat ai bolii vasculare21,23,24, precum și cu evenimentele cardiovasculare25 și mortalitatea de orice cauză22. În plus, studiile de laborator au furnizat mecanisme plauzibile prin care CPP poate media aceste rezultate vasculare patologice26-28. Cu toate acestea, în timp ce studiile in vitro au sugerat că multe dintre aceste toxicități sunt induse într-o manieră dependentă de doză, dacă CPP are un rol fiziologic normal în sănătate, nu este clar în ce moment aceste particule pot deveni dăunătoare. Cunoașterea efectului aportului nutrițional asupra cineticii CPP, așa cum este dezvăluită aici, se poate dovedi crucială pentru înțelegerea în continuare a acestui proces. O concentrație de prag pentru apariția efectelor patologice ale CPM și CPP poate fi atinsă (cel puțin inițial) numai în starea postprandială in vivo. Dacă da, testarea dinamică a răspunsului post-prandial poate oferi oportunități suplimentare de a evalua manifestările anterioare ale metabolismului mineral dereglat, precum și riscul de boală vasculară asociată. O altă posibilitate importantă este că compoziția și, prin urmare, toxicitatea intrinsecă a CPP-I și CPP-II diferă între sănătate și CKD45.

Supliment Cistanche
Limitări
Recunoaștem că acest studiu are mai multe limitări, inclusiv un număr limitat de pacienți, așa cum sa discutat deja. În special, am folosit și o masă standardizată dată după un post peste noapte, așa că nu putem comenta efectul variației compoziției mesei sau efectul meselor ulterioare date în restul zilei. Am ales masa pe baza disponibilității sale comerciale, permițând standardizarea între participanți și pentru că reprezenta încărcături nutriționale relevante din punct de vedere fiziologic (Tabelul 1). Cu toate acestea, este posibil ca, dacă participanții au fost provocați cu încărcături minerale mai mari, o separare suplimentară între cei cu funcție renală normală și afectată ar fi putut fi evidentă. În mod similar, având în vedere că am observat indivizi doar timp de patru ore după masă, este posibil ca efectul cumulativ al meselor ulterioare să fi distins și mai mult grupurile.
Nu am recuperat fecale sau urină și, prin urmare, nu putem comenta totalul de minerale absorbite sau excretate în timpul studiului. Presupunem că modificările în fiecare măsură observate după hrănire sunt direct legate de aportul nutrițional. Această ipoteză este susținută indirect de studii imagistice detaliate care arată fux de ioni de calciu și fosfat în urma consumului de alimente57, precum și dovezi directe din studiile pe animale care arată că gavajul oral acut la șoareci cu o soluție tamponată de fosfat are ca rezultat creșteri serice în CPM/CPP48. Cu toate acestea, nu am observat participanții în condiții de post prelungit și, prin urmare, nu putem explica în mod concludent fluctuațiile diurne care nu sunt legate de alimentație în niciunul dintre parametrii studiați. Cu toate acestea, am avut două eșantioane de post, a căror medie a fost folosită ca „timp 0”, iar variabilitatea dintre aceste eșantioane de post a fost trivială în comparație cu amploarea modificărilor observate în perioada postprandială.
Am folosit metoda Bonferroni pentru a ține cont de multiplele comparații post-hoc perechi între și în cadrul grupurilor pentru fiecare parametru. Aceasta este, fără îndoială, o abordare conservatoare și, după cunoștințele noastre, nu a fost adoptată de niciun alt studiu similar asupra metabolismului mineral postprandial. Am ales această abordare având în vedere numărul mare de momente și comparații care au fost făcute și am motivat că este de preferat să ne concentrăm pe semnalele cele mai robuste și semnificative. Cu toate acestea, ca rezultat, este posibil să fi ratat efecte mai mici, dar potențial relevante. Nu am corectat teste multiple pentru diferiți parametri minerali, având în vedere probabilitatea unor modificări interdependente legate fiziologic.

Cistanche tubulosa
Concluzie
Studiul nostru a dezvăluit pentru prima dată că aportul de minerale nutriționale duce la formarea CPM și CPP în sânge ca răspuns fiziologic normal la hrănire. Aceste constatări coroborează ipoteza conform căreia formarea CPM/CPP ajută la formarea încărcăturilor minerale postprandiale, funcționând ca un depozit temporar circulant de fosfați de calciu în vrac, destinați în cele din urmă utilizării/stocării (de exemplu, un precursor mineral pentru mineralizarea osoasă) sau eliminare. Am observat, de asemenea, niveluri mai mari de CPM seric și un răspuns post-prandial mai mare la cei cu funcție renală afectată, sugerând că metabolismul CPM este alterat în mod evident în CKD. Analiza manipulării CPM/CPP post-prandială poate oferi noi perspective asupra mecanismelor care leagă aportul excesiv de calciu și fosfat alimentar cu riscuri crescute de boli cardiovasculare la pacienții cu excreție minerală afectată. Mai larg, aceste descoperiri noi subliniază contribuția importantă, dar adesea neglijată, a biochimiei coloidale la homeostazia minerală.
Referințe
1. Magalhães, MCF, Marques, PAAP & Correia, RN Biomineralization—Medical Aspects of Solubility (eds. Königsberger, E. & Königsberger, L.). 71–123. (Wiley, 2006).
2. Holt, C., Lenton, S., Nylander, T., Sorensen, ES & Teixeira, SC Mineralizarea țesuturilor moi și dure și stabilitatea biofluidelor. J. Struct. Biol. 185, 383–396 (2014).
3. Reznikov, N., Steele, JAM, Fratzl, P. & Stevens, MM O viziune a științei materialelor asupra mineralizării matricei extracelulare. Nat. Pr. Mater. 1, 16041 (2016).
4. Smith, ER Calcificarea vasculară în uremie: concepte New-age despre o problemă a bătrâneții. Metode Mol. Biol. 1397, 175–208 (2016).
5. Chen, J. şi colab. Calcificarea arterei coronare și riscul de boli cardiovasculare și deces în rândul pacienților cu boală renală cronică. JAMA Cardiol. 2, 635–643 (2017).
6. Kestenbaum, BR și colab. Incidența și progresia calcificării coronariene în boala cronică de rinichi: Studiul multietnic al aterosclerozei. Rinichi Int. 76, 991–998 (2009).
7. Isakova, T. şi colab. Metabolismul mineral postprandial și hiperparatiroidismul secundar în CKD precoce. J. Am. Soc. Nefrol. 19, 615–623 (2008).
8. Scanni, R., vonRotz, M., Jehle, S., Hunter, HN & Krapf, R. Răspunsul uman la încărcările acute de fosfat enterale și parenterale. J. Am. Soc. Nefrol. 25, 2730–2739 (2014).
9. Pasch, A., Jahnen-Dechent, W. & Smith, ER Fosfat, calcificare în sânge și stres mineral: sistemul fiziologic de tamponare a mineralelor din sânge și asocierea sa cu riscul cardiovascular. Int. J. Nephrol. 2018, 9182078 (2018).
10. Jahnen-Dechent, W. şi colab. Nămol în sânge: Rolul complexelor proteine-minerale și al veziculelor extracelulare în biomineralizare și calcificare. J. Struct. Biol. 212, 107577 (2020).
11. Schinke, T. şi colab. Proteina serică alfa2-HS glicoproteina/fetuina inhibă formarea apatitei in vitro și mineralizarea celulelor calvariei. Un posibil rol în mineralizarea și homeostazia calciului. J. Biol. Chim. 271, 20789–20796 (1996).
12. Heiss, A. et al. Baza structurală a inhibării calcificării de către glicoproteina alfa 2-HS/fetuina-A. Formarea particulelor de calciproteine coloidale. J. Biol. Chim. 278, 13333–13341 (2003).
13. Cai, MM, Smith, ER & Holt, SG Rolul fetuinei-A în traficul și depunerea mineralelor. Bonekey Rep. 4, 672 (2015).
14. Smith, ER, Hewitson, TD și Jahnen-Dechent, W. Particule de calciproteine: minerale care se comportă rău? Curr. Opinează. Nefrol. Hipertens. 29, 378–386 (2020).
15. Jahnen-Dechent, W., Schäfer, C., Ketteler, M. & McKee, MD Chaperone minerale: un rol pentru fetuin-A și osteopontin în inhibarea și regresia calcificării patologice. J. Mol. Med. (Berl.) 86, 379–389 (2008).
16. Jahnen-Dechent, W. & Smith, ER Remediul naturii pentru problemele legate de fosfat: Particulele de calciproteine reglează metabolismul mineral sistemic. Rinichi Int. 97, 648–651 (2020).
17. Schafer, C. şi colab. Proteina serică alfa 2-Glicoproteina/fetuina-A Heremans-Schmid este un inhibitor sistemic al calcificării ectopice. J. Clin. Investi. 112, 357–366 (2003).
18. Herrmann, M. şi colab. Calcificarea lumenă și micro-vasculopatia la șoarecii cu deficit de fetuină A duc la morbiditate de organe multiple. PLoS ONE 15, e0228503 (2020).
19. Heiss, A., Pipich, V., Jahnen-Dechent, W. & Schwahn, D. Fetuin-A este o proteină purtătoare de minerale: împrăștierea neutronilor cu unghi mic oferă o nouă perspectivă asupra inhibării controlate a calcificării Fetuin-A. Biophys. J. 99, 3986–3995 (2010).
20. Smith, ER şi colab. Concentrația serică de fetuină-A și particule de calciproteină care conțin fetuină-A la pacienții cu boală inflamatorie cronică și insuficiență renală. Nefrologie (Carlton) 18, 215–221 (2013).
21. Smith, ER şi colab. Particulele de calciproteină fosforilate care conțin fetuină A sunt asociate cu rigiditatea aortică și un mediu prociclic la pacienții cu CKD pre-dializă. Nefrol. Apelează. Transplant. 27, 1957–1966 (2012).
22. Smith, ER şi colab. Propensiunea de calcificare a serului prezice mortalitatea de toate cauzele în CKD predializă. J. Am. Soc. Nefrol. 25, 339–348 (2014).
23. Hamano, T. şi colab. Complexul fetuină-mineral reflectă stresul de calcificare extraosă în CKD. J. Am. Soc. Nefrol. 21, 1998–2007 (2010).
24. Nakazato, J. et al. Asocierea particulelor de calciproteină măsurată printr-o nouă metodă cu placa de arteră coronară la pacienții cu boală coronariană: un studiu transversal. J. Cardiol. 74, 428–435 (2019).
25. Gatate, Y. et al. Valoarea predictivă pe termen mediu a particulelor de calciproteină la pacienții cu hemodializă de întreținere pe baza unui test de filtrare cu gel. Ateroscleroza 303, 46–52 (2020).
26. Cai, MMX, Smith, ER, Tan, SJ, Hewitson, TD & Holt, SG Rolul particulelor secundare de calciproteine în paradoxul de mineralizare al bolii cronice de rinichi. Calcif. Țesut. Int. 101, 570–580 (2017).
27. Aghagolzadeh, P. et al. Calcificarea celulelor musculare netede vasculare este indusă de particulele secundare de calciproteină și sporită de factorul de necroză tumorală alfa. Ateroscleroza 251, 404–414 (2016).
28. Koppert, S. şi colab. Clearance-ul celular și activitatea biologică a particulelor de calciproteină depind de starea lor de maturare și de cristalinitate. Față. Imunol. 9, 1991 (2018).
29. Koeppert, S. şi colab. Imagistica live a clearance-ului particulelor de calciproteină și a absorbției mediate de receptor: rolul monomerilor calciproteici. Față. Celulă. Dev. Biol. 9, 633925 (2021).
30. Shishkova, D. et al. Bionii de fosfat de calciu provoacă hiperplazie intimă în aortele intacte ale șobolanilor normolipidemici prin leziuni endoteliale. Int. J. Mol. Sci. 20, 5728 (2019).
31. Kuro-o, M. O paradigmă centrată pe fosfat pentru patofiziologia și terapia bolii cronice de rinichi. Rinichi Int. Supl. 2011(3), 420–426 (2013).
32. Miura, Y. et al. Identificarea și cuantificarea particulelor de calciproteine plasmatice cu proprietăți fizice distincte la pacienții cu boală renală cronică. Sci. Rep. 8, 1256 (2018).
33. Smith, ER et al. Un nou test fluorescent pe bază de citometrie în flux pentru nanoparticulele care conțin minerale în ser. Sci. Rep. 7, 5686 (2017).
34. Nakamura, K. et al. Efectul carbonatului de lantan asupra particulelor de calciproteină la pacienții cu hemodializă. Clin. Exp. Nefrol. 24, 323–329 (2020).
35. Tiong, MK și colab. Efectul unei tăieturi medii a dializatorului asupra toxinelor uremice legate de proteine și a markerilor de metabolism mineral la pacienții aflați în hemodializă. Hemodial. Int. https://doi.org/10.1111/hdi.12924 (2021).
36. Tiong, MK, Smith, ER, Toussaint, ND, Al-Khayyat, HF & Holt, SG Reducerea particulelor de calciproteină la adulții care primesc infliximab pentru boala inflamatorie cronică. JBMR Plus 5, e10497 (2021).
37. Smith, ER, Pan, FFM, Hewitson, TD, Toussaint, ND & Holt, SG Efectul sevelamerului asupra particulelor de calciproteină la pacienții cu hemodializă: Te sevelamer versus calciu pentru a reduce particulele de calciproteină care conțin fetuină A în dializă (SCaRF) randomizat proces controlat. Rinichi Int. Rep. 5, 1432–1447 (2020).
38. Ruderman, I., Smith, ER, Toussaint, ND, Hewitson, TD & Holt, SG Modificări longitudinale ale metabolismului osos și mineral după încetarea tratamentului cu cinacalcet la pacienții dializați cu hiperparatiroidism secundar. BMC Nephrol. 19, 113 (2018).
39. Bressendorf, I. et al. Efectul creșterii magneziului de dializat asupra particulelor de calciproteine, a inflamației și a markerilor osos: analiză post-hoc dintr-un studiu clinic controlat randomizat. Nefrol. Apelează. Transplant. 36, 713–721 (2021).
40. Pasch, A. şi colab. Testul pe bază de nanoparticule măsoară tendința generală de calcificare în ser. J. Am. Soc. Nefrol. 23, 1744–1752 (2012).
41. Eelderink, C. și colab. Propensiunea de calcificare a serului și riscul de mortalitate cardiovasculară și de toate cauzele în populația generală: Studiul PREVENT. Arterioscler. Tromb. Vasc. Biol. 40, 1942–1951 (2020).
42. Bundy, JD et al. Propensiunea de calcificare a serului și calcificarea arterei coronare în rândul pacienților cu CKD: studiu Te CRIC (Chronic Renal Insufficiency Cohort). A.m. J. Rinichi. Dis. 73, 806–814 (2019).
43. Bundy, JD et al. Propensiunea de calcificare a serului și evenimentele clinice în CKD. Clin. J. Am. Soc. Nefrol. 14, 1562–1571 (2019).
44. Pasch, A. şi colab. Înclinația la calcificarea sângelui, evenimentele cardiovasculare și supraviețuirea la pacienții care primesc hemodializă în studiul EVOLVE. Clin. J. Am. Soc. Nefrol. 12, 315–322 (2017).
45. Smith, ER, Hewitson, TD, Hanssen, E. & Holt, SG Transformarea biochimică a particulelor de calciproteină în uremie. Bone 110, 355–367 (2018).
46. Chen, W. şi colab. Asocierea dimensiunii particulelor calciproteinei serice și a timpului de transformare cu calcificarea arterială, rigiditatea arterială și mortalitatea la pacienții cu hemodializă incidente. A.m. J. Rinichi Dis. 77, 346–354 (2021).
47. Chen, W. şi colab. Pacienții cu boală renală cronică avansată și calcifiere vasculară au o rază hidrodinamică mare a particulelor secundare de calciproteină. Nefrol. Apelează. Transplant. 34, 992–1000 (2019).
48. Akiyama, KI et al. Particulele de calciproteină reglează expresia factorului de creștere-23 a fibroblastelor în osteoblaste. Rinichi Int. 97, 702–712 (2020).
49. Smith, ER Particule de calciproteină: un biomarker mineral care necesită o măsurătoare mai bună. Ateroscleroza 303, 43–45 (2020).
50. Smith, ER Izolarea și cuantificarea particulelor de calciproteină care conțin fetuină-A din fluide biologice. Metode Mol. Biol. 1397, 221–240 (2016).
51. Guo, Y., Logan, HL, Glueck, DH & Muller, KE Selectarea unei dimensiuni a eșantionului pentru studii cu măsuri repetate. BMC Med. Res. Metoda. 13, 100 (2013).
52. Liu, C., Cripe, TP & Kim, MO Probleme statistice în analiza longitudinală a datelor pentru studiile de eficacitate a tratamentului în științele biomedicale. Mol. Ter. 18, 1724–1730 (2010).
53. Tobin, J. Estimarea relațiilor pentru variabile dependente limitate. Econometria 26, 24–36 (1958).
54. Ter Meulen, KJ et al. Dializatul de acid citric îmbunătățește predispoziția la calcifiere a pacienților cu hemodializă: un studiu multicentric, prospectiv, randomizat încrucișat. PLoS ONE 14, e0225824 (2019).
55. Tiem, U. et al. Efectul terapiei cu lianți de fosfat cu oxihidroxid sucroferric asupra tendinței de calcificare la pacienții cu hemodializă cronică: un studiu randomizat, controlat, încrucișat. Clin. Kidney J. 14, 631–638 (2021).
56. Yamada, H. şi colab. Variabilitatea zilnică a nivelurilor serice ale particulelor de calciproteină și asocierea lor cu parametrii de metabolism mineral: un studiu pilot transversal. Nefrologie (Carlton) 23, 226–230 (2018).
57. Stremke, ER et al. Absorbția intestinală a fosforului la CKD moderată și la adulții sănătoși a fost determinată folosind un trasor radioizotopic. J. Am. Soc. Nefrol. 32, 2057–2069 (2021).
58. Volk, C. şi colab. Efectele acute ale unui aditiv de fosfor anorganic asupra metabolismului mineral și a factorilor de risc cardiometabolici la subiecții sănătoși. J. Clin. Endocrinol. Metab. 107, e852–e864 (2022).
59. Turner, ME și colab. Toleranța afectată la fosfat a fost evidențiată cu o provocare orală acută. J. Minerul de oase. Res. 33, 113–122 (2018).
60. Tomas, L. et al. Adaptarea acută la fosfat oral sau intravenos necesită hormon paratiroidian. J. Am. Soc. Nefrol. 28, 903–914 (2017).
61. Zelt, JG şi colab. Depunerea acută de minerale tisulare ca răspuns la un impuls de fosfat în CKD experimentală. J. Minerul de oase. Res. 34, 270–281 (2019).
62. Lebreton, JP şi colab. Concentrația serică a alfa 2 HS glicoproteinei umane în timpul procesului inflamator: dovezi că alfa 2 HS glicoproteinei este un reactant negativ în fază acută. J. Clin. Investi. 64, 1118–1129 (1979).
63. Uedono, H. şi colab. Efectele particulelor de calciproteină care conțin fetuină-A asupra modificărilor post-translaționale ale fetuinei-A în celulele HepG2. Sci. Rep. 11, 7486 (2021).
64. Niv, Y. & Fraser, GM Te fenomenul mareelor alcaline. J. Clin. Gastroenterol. 35, 5–8 (2002).
65. Smith, ER, Hewitson, TD & Holt, SG Teste diagnostice pentru calcificarea vasculară. Adv. Dis. renală cronică. 26, 445–463 (2019).
66. Sprague, SM și colab. Acuratețea diagnosticului markerilor de turnover osos și histologiei osoase la pacienții cu BRC tratați prin dializă. A.m. J. Rinichi Dis. 67, 559–566 (2016).
67. Vorland, CJ și colab. Progresia bolii renale nu scade absorbția intestinală a fosforului într-un model de șobolan de boală renală cronică - tulburare osoasă minerală. J. Minerul de oase. Res. 35, 333–342 (2020).
68. Marks, J. şi colab. Absorbția intestinală a fosfatului într-un model de insuficiență renală cronică. Rinichi Int. 72, 166–173 (2007).
69. Hill Gallant, KM & Vorland, CJ Absorbția intestinală a fosforului: descoperiri recente în cercetarea translațională și clinică. Curr. Opinează. Nefrol. Hipertens. 30, 404–410 (2021).
70. Herrmann, M. şi colab. Eliminarea particulelor de calciproteină care conțin fetuină-A este mediată de receptorul scavenger-A. Circ. Res. 111, 575–584 (2012).
71. Compania Sanitarium Health Food. Aroma de gheață de vanilie UP&GO™. https://www.sanitarium.com.au/products/up-and-go/up-and-go/vanilla-ice-favor (2021).
72. Guvernul Australian National Health and Medical Research Council. Valori de referință pentru nutrienți pentru Australia și Noua Zeelandă. https://www.nrv.gov.au/nutrients (2021).
Mark K.Tiong1,2, Michael MX Cai1 , Nigel D.Toussaint1,2, Sven‑JeanTan1,2, Andreas Pasch3,4,5 & Edward R. Smith1,2
1 Departamentul de Nefrologie, Spitalul Royal Melbourne, Strada Grattan, Parkville, VIC 3052, Australia.
2 Departamentul de Medicină (RMH), Universitatea din Melbourne, Parkville, Australia.
3 Calciscon AG, Biel, Elveția.
4 Lindenhofspital Bern, Berna, Elveția.
5 Departamentul de Fiziologie și Fiziopatologie, Universitatea Johannes Kepler, Linz, Austria.






