Glicozide totale de Cistanche Deserticola promova neurologice funcția de recuperare prin inducerea regenerarea neurovasculare prin nrf- 2/Keap-1 calea în MCAO/R șobolani
Mar 03, 2022
Persoană de contact: Audrey Hu Whatsapp / hp: 0086 13880143964 e-mail:audrey.hu@wecistanche.com
Fujiang Wang , Ruiyan Li , Pengfei Tu , Jianping Chen , Kewu Zeng și Yong Jiang
Fond:Medicina tradițională chineză Cistanche deserticola a fost raportat a fi valabil pentru boli cardiovasculare și cerebrovasculare. Cu toate acestea, componentele sale active pentru protecția accidentului vascular cerebral ischemic nu sunt clare. Ne-am propus să explorăm componentele active aleC. deserticolaîmpotriva accident vascular cerebral ischemic, precum și mecanismele sale potențiale.Metode:Am investigat efectele protectoare ale creierului ale extractelor din extracteC. deserticola, glicozide totale (TG), polizaharide (PSs) și oligozaharide (OSs) într-un model de șobolan de ocluzie-reperfuzie a arterei cerebrale medii (MCAO/R). 2, 3, 5-trifenil clorură de tetrazoliu (TTC) colorare a fost folosit pentru a evalua volumul infarctului cerebral, și Evans test albastru a fost adoptat pentru a evalua bariera sange - creier (BBB) permeabilitatea. Apoi, expresiile CD31, a-SMA, PDGFRb, SYN, PSD95, MAP-2, ZO-1, claudin-5, ocludin, Keap-1 și Nrf-2 au fost analizate folosind blotting-ul vestic sau imunofluorescența, iar activitățile MDA, SOD, CAT și GSH-Px au fost analizate folosind kituri.Rezultatele:Tratamentul TGs a scăzut remarcabil scorurile deficitului neurologic și volumele de infarct, a promovat angiogeneza și remodelarea neuronală și a menținut în mod eficient integritatea barierei hemato-encefalice în comparație cu grupul model. În plus, TGs a scăzut semnificativ nivelurile de MDA și a crescut activitățile antioxidante (SOD, CAT, și GSH-Px) în creiere. Între timp, TGs a retrogradat remarcabil expresia Keap-1 și a facilitat translocarea nucleară Nrf-2. Dimpotrivă, nu s-au observat efecte protectoare pentru grupurile PSs și OSs.Concluzie:TGs sunt principalele componente active aleC. deserticolaîmpotriva leziunilor cerebrale induse de MCAO/R, iar protecția este în principal prin calea Nrf-2/Keap-1.
Cuvinte-cheie: Cistanche deserticola, leziuni cerebrale, glicozide totale, polizaharide, oligozaharide, Nrf-2/Keap- 1 cale

INTRODUCERE
Accidentele vasculare cerebrale sunt considerate a fi o cauză majoră de deces și invaliditate în lume (Donnan et al., 2008). Aproape 87% din toate cazurile de accident vascular cerebral sunt declanșate de accident vascular cerebral ischemic (Ovbiagele și Nguyen-Huynh, 2011). În prezent, cel mai eficient agent și singurul medicament aprobat de FDA utilizat pentru tratamentul accidentului vascular cerebral ischemic este activatorul plasminogen al țesutului recombinant. Cu toate acestea, un număr mare de pacienți cu accident vascular cerebral nu reușesc să răspundă la acest medicament, din cauza ferestrei sale de timp terapeutice înguste și a unui risc grav de complicații hemoragice (Lee et al., 2012; Schellinger și Kohrmann, 2014). O provocare majoră a tratamentului trombolitic este ischemia/reperfuzia (I/R), care este considerată principala cauză a leziunilor cerebrale și a distrugerii funcției. Reperfuzia după ischemie cerebrală crește riscul unei hemoragii cerebrale, ducând în același timp la leziuni neurovasculare și producând specii excesive reactive de oxigen (ROS) care dăunează barierei hemato-encefalice (Alluri et al., 2015). Mai multe studii au confirmat că perturbarea BBB este o cauză majoră a patogenezei accidentului vascular cerebral ischemic (Cao et al., 2016b).
BBB constă în principal din celule endoteliale, pericite, astrocite, neuroni și membrane subsol. Componentele de bază ale BBB sunt celulele endoteliale microvasculare cerebrale care sunt unite prin joncțiuni strânse, restricționând astfel moleculele exogene în creier. Modificările patologice ale joncțiunilor strânse - în special ocludin, claudin-5 și zonula ocludens-1 (ZO-1) - afectează în mod semnificativ funcția BBB în timpul unui accident vascular cerebral ischemic, în special permeabilitatea barierei (Liu et al., 2014; Hu et al., 2018; Liu et al., 2019). În timpul perioadelor I/R, ROS excesiv este unul dintre principalii factori care conduc la deteriorarea directă a neuronilor creierului (Ding et al., 2014). Supraproducția ROS duce la degradarea anumitor joncțiuni și la perturbarea BBB, ceea ce duce la intrarea moleculelor exogene în creier prin BBB, ceea ce duce la agravarea leziunilor cerebrale (Cheon et al., 2016; Zhang Q. Y. et al., 2017). Prin urmare, protecția BBB de anti-oxidanți a fost considerată ca o modalitate potențială de a preveni reperfuzie prejudiciu.
Pe lângă defalcarea BBB, I/R poate duce la leziuni neurovasculare și moarte neuronală (Jung et al., 2010). În timpul unui accident vascular cerebral, moartea crescută a celulelor neuronale poate rezulta din stresul oxidativ (Chi et al., 2018), iar numeroase studii au arătat că ROS agravează severitatea accidentului vascular cerebral și leziunile neurologice (Kondo et al., 1997; Crack et al., 2001; Crack et al., 2006). Deși studiile clinice nu au obținut rezultate satisfăcătoare, neuroprotecția este încă o strategie promițătoare pentru tratamentul accidentului vascular cerebral ischemic acut (Moretti et al., 2015). Astfel, găsirea unor medicamente eficiente de neuroprotecție pentru tratarea accidentelor vasculare cerebrale este un beneficiu pentru pacienții cu accident vascular cerebral.
Medicina tradițională chineză (TCM) ia măsuri pentru a interveni împotriva dezechilibrului intern al organismului (Gaire, 2018). Datorită patogenezei complexe a accidentelor vasculare cerebrale ischemice, efectul multifactorial al TCM și constituenții săi activi joacă un rol critic în tratamentul accidentelor vasculare cerebrale. Cistanche deserticola Y. C. Ma, răspândită în zonele aride sau semi-aride în mongolia și nord-vestul Chinei, a fost o plantă TCM utilizată pe scară largă pentru tratamentul diferitelor boli, cum ar fi uitarea și depresia pentru mai mult de 1.000 de ani în China. Modernstudiile farmacologice au indicat că extractele brute dinC. deserticolaa arătat mai multe activități farmacologice, cum ar fi îmbunătățirea funcției de învățare și memorie, neuroprotecție, îmbunătățirea imunității, efecte antioxidante, anti-îmbătrânire și antifatigue (Ko și Leung, 2007; Wang et al., 2012; Li et al., 2015). Analiza chimică a C. deserticola a arătat că principalele sale constituie includ glicozide feniletanoide, glicozide iridoide, polizaharide, și oligozaharide (Jiang și Tu, 2009). Cu toate acestea, componentele active ale C. deserticola pentru protecția creierului nu sunt foarte clare.Proprietatea neuroprotectoare a C. deserticola implică potențialul său terapeutic în boli legate de cognitiv, cum ar fi accidentul vascular cerebral și depresia, precum și boala Alzheimer (Wang et al., 2017). Cu toate acestea, cercetări privind impactulC. deserticolape accidente vasculare cerebrale, inclusiv componentele sale active și mecanismele de acțiune, este foarte limitată. În activitatea curentă, am explorat efectul protector a trei extracte din C. deserticola, glicozide totale (TGs, glicozide feniletanoide și alte glicozide), polizaharide (PSs) și oligozaharide (OS) asupra leziunilor cerebrale I/R. Constatările noastre pot contribui la aplicarea clinică exactă aC. deserticolași să ofere un agent candidat pentru terapia accident vascular cerebral ischemic.

MATERIALE ȘI METODE
Substanțe chimice și reactivi
Tulpinile de Cistanche deserticola au fost cumpărate de la Alashan, Mongolia Interioară, și identificate de către unul dintre autori (P.-F. Tu). TGs, PSs și OSs au fost pregătite în conformitate cu metoda raportată anterior de Curte (Gao et al., 2015). Analiza cantitativă a TG a fost efectuată prin cromatografie lichidă de înaltă performanță (HPLC), astfel cum a fost descrisă anterior (Li et al, 2019), iar cromatograma sa este prezentată în figura 1. Principalele componente ale TGs sunt echinacozida, tubuloside A, acteosidă, izo-acteozidă și 2'-acetilacteozidă; conținutul lor este de 163,05 mg/g, 4,125 mg/g, 41,66 mg/g, 22,655 mg/g și, respectiv, 12,045 mg/g. Conținutul PSs și OSs este de 69,42% și, respectiv, 65,24%, determinat de HPLC și, respectiv, de analiza acidului fenol-sulfuric (Zhang A. et al., 2018; Shi et al, 2019).
Referințele standard ale echinacozidei (A0282), tubulozidei A (A0942), actelorozidei (A0280), izo-acteozidei (A0281) și 2'- acetilacteozidei (A0943) au fost achiziționate de la Chengdu Must Biotechnology (Sichuan, China). Puritatea tuturor standardelor este mai mare de 98%. Kiturile Nissl stain H&E au fost cumpărate de la Boster (Wuhan, China). Edaravone (T0407-1) a fost cumpărat de la Target Mol (Shanghai, China). Iepure anti-șobolan MAP-2 (ab32454), Nrf-2 (ab31163), PDGFRb (ab32570), Keap-1 (ab66620), și mouse-ul anti-șobolan CD31 (ab24590) au fost achiziționate de la Abcam Inc (Cambridge, MA, SUA). Iepurele anti-șobolan Claudin5 (BS1069), ZO-1 (BS9802M) și Occludin (BS72035) au fost cumpărate de la Bioworld Technology (Nanjing, China). Cell Signaling Technology Inc. (Boston, MA, SUA) a fost sursa de iepure anti-șobolan Synapsin-1 (SYN,5297T), PSD95 (3450T), a-Smooth Muscle Actin (a-SMA,19245T). GAPDH (HRP-60004) a fost achiziționat de la Proteintech Group, Inc. (Chicago, SUA). Anticorpii secundari au fost furnizați de Zhongshan Golden Bridge Biotechnology (Beijing, China). Hoechst 33258 a fost obținută de la Beyotime (Jiangsu, China).
Animale
Șobolanii Sprague-Dawley (masculi, cu o greutate de 250-300g) au fost obținuți de la Vital River Laboratory Animal Technology (Beijing, China) și adăpostiți într-o cameră cu aer condiționat, păstrată pe un ciclu de lumină/întuneric de 12 ore. Toate experimentele pe animale au fost efectuate de către liniile directoare de cercetare pe animale SOS (Kilkenny et al., 2010; McGrath et al., 2010), și aprobat de comitetul instituțional de îngrijire și utilizare a animalelor al Peking University Health Science Center (LA2019123).
Protocoale experimentale pe animale
Șobolanii au fost supuși MCAO/R, așa cum s-a descris anterior (Wang et al., 2018). Pe scurt, artera carotidă comună stângă (CCA), artera carotidă externă (ECA) și artera carotidă internă (ICA) au fost expuse și o sutură monofilament de nailon 3-0 a fost introdusă din CCE în ICA până la atingerea arterei cerebrale medii (MCA). După 1,5 ore de ocluzie MCA, reperfuzia a fost simulată prin îndepărtarea filamentului. În timpul procedurii chirurgicale, temperatura corpului tuturor șobolanilor a fost menținută la 37,0 °C.
Administrarea medicamentelor
Șobolanii au fost separați aleatoriu în șase grupuri folosind versiunea software SPSS 22.0 așa cum este descris (Jiang et al., 2014): grup normal (NOR); grup model (MOD); Grupul edaravonei (medicament pozitiv, 6 ml/kg, EDI); Grupul TGs (280 mg/kg, TGs); Grupul PSs (280 mg/kg, PSs) și grupul OSS (280 mg/kg, OS). TGs, PSs, și sisteme de operare au fost administrate o dată pe zi după MCAO / R timp de 14 zile. Grupurile NOR și MOD au fost tratate cu soluție salină normală. Numerele animalelor sunt prezentate în tabelul 1.

Măsurarea greutății și a scorurilor deficitului neurologic modificat (mNSS)
Greutatea corporală a fost monitorizată în a 14-a zi folosind o scală digitală ADVENTURE™ (OHAUS, New Jersey, SUA). MNSS a fost evaluat conform metodei descrise de FJ Wang (Wang et al., 2018), cu revizuiri minore.
2, 3, 5-Triphenyltetrazolium Clorură (TTC) Colorare
Volumul infarctului a fost măsurat așa cum a fost descris anterior (Wang et al., 2015). Pe scurt, creierul a fost secționat în șapte blocuri coronale la fel de distanțate (2 mm). Aceste secțiuni au fost colorate cu 2% TTC (Coolaber, Beijing, China) la 37 ° C timp de 15 min. Volumul infarctului (%) = (volumul emisferei ischemice ipsilaterale −volumul emisferei ischemice contralaterale)/volumul emisferei ischemice contralaterale × 100.
Nissl și H & E colorare
Șobolanii au fost profund anesteziați, iar întregul creier a fost apoi scos rapid din craniu și fixat folosind 4% paraformaldehidă și încorporat în ceară de parafină și secționat în felii de grosime de 7 μm. Secțiunile au fost colorate cu Nissl și H&E. În acest studiu, șase câmpuri aleatorii de 200 × 200 μm au fost capturate în fiecare probă de țesut cu un microscop ușor. Numărul de corpuri ale lui Nissl a fost numărat cu software-ul IPP versiunea 6.0 (Media Cybernetics, Bethesda, SUA).
Evans Blue Test
Șobolanii au fost injectați cu 2% EB (Coolaber Science & Technology Co., LTD) după MCAO/R. Două ore mai târziu, șobolanii au fost anesteziați și întregul creier a fost apoi îndepărtat rapid și omogenizat în acetonă. Supernatanții au fost analizați la 620 nm de un cititor de absorbanță 800 TS (BioTek, SUA).
Măsurarea activităților de catalază (CAT), superoxid dismutază (SOD), malondialdehidă (MDA) și glutation peroxidază (GSH-Px)
Toate probele de ser au fost centrifugate la 4.000 × rpm timp de 15 minute la 4 °C și apoi analizate pentru a detecta activitățile MDA, CAT, SOD și GSH-Px urmând instrucțiunile producătorului (Jiangsu Meimian Industrial Co., Ltd, China).
Western Blotting Analiza
Țesuturile cerebrale (100 mg) colectate de la fiecare șobolan au fost omogenizate și lizate în tampon de liză RIPA și apoi analizate pentru a detecta concentrația proteinelor folosind un kit BCA (Beijing TransGen Biotech Co., Ltd.). Proteinele totale ale țesuturilor au fost încărcate pe geluri SDS-PAGE 10% și transferate pe o membrană de nitroceluloză. Membrana a fost blocată folosind 5% lapte degresat, apoi incubată peste noapte cu anticorpi primari la 4°C. Membrana a fost apoi incubată cu un anticorp secundar. Analiza Western blot a fost analizată folosind Kodak Digital Imaging System (5200 Multi, Tanon, China).
Analiza imunofluorescentă
Au fost efectuate colorarea imunofluorescenței pentru CD31, a-SMA, ZO-1, claudin5, ocludină, PDGFRb, SYN, PSD95, MAP-2, Nrf-2 și Keap-1. Anticorpii primari împotriva Nrf-2, CD31, a-SMA, ZO-1, claudin5, ocludin, PDGFRb, SYN, PSD95, MAP-2 și Keap-1 au fost diluați la 1:200 și, respectiv, 1:100. Anticorpul secundar al Alexa Flur 488 mouse anti-iepure IgG și rodamină (TRITC) capră anti-iepure IgG au fost diluate la 1:200. Nucleele au fost colorate de Hoechst 33258. Imaginile au fost surprinse cu ajutorul sistemului automat de imagistică cantitativă a patologiei Vectra® Polaris™ (PerkinElmer, SUA). Expresia proteinelor a fost analizată folosind software-ul IPP versiunea 6.0.
Analiza statistică
Toate datele au fost descrise ca medie ± SD. SPSS software versiunea 22.0 a fost efectuată pentru analiza statistică. ANOVA unidirecțională a fost utilizată atunci când se compară diferite grupuri. P< 0.05="" was="" considered="" to="" be="" the="" statistical="">
REZULTATELE
TGs crește greutatea corporală și reduce daunele cerebrale în ȘOBOLANI MCAO/R
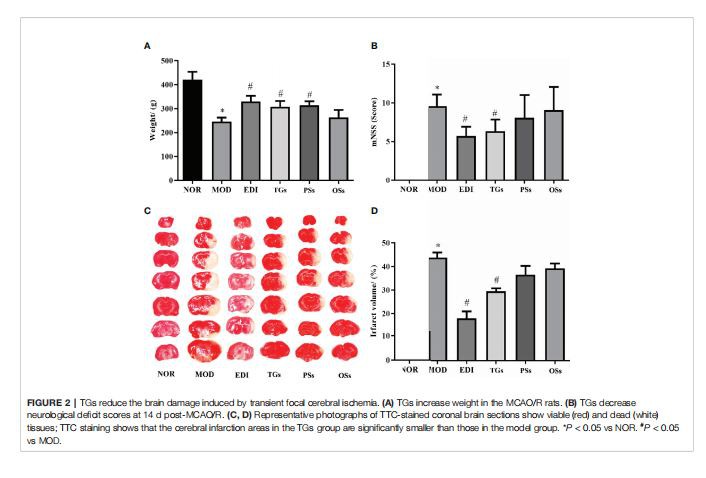
După 14 zile de vindecare cu TGs, PSs, Oss și EDI, au fost evaluate greutățile corporale, deficitele neurologice și volumele de infarct ale șobolanilor I/R. Rezultatele au arătat că ponderile corporale din grupul MOD au scăzut foarte mult, în timp ce ponderile scăzute în grupurile TGs, PSs și EDI au fost crescute (Figura 2A). Scorurile deficitului neurologic au fost reduse substanțial de EDI și TG (Figura 2B). Feliile cerebrale la șobolanii din grupul NOR au fost de culoare roșie profundă și nu au existat infarcte, în timp ce șobolanii din grupul MOD au prezentat un infarct cerebral ipsilateral mare. După tratamentul cu TGs, volumele infarctului au fost reduse semnificativ(Figurile 2C, D). Tratamentul PSs și OSs nu a arătat nici un efect evident asupra indicilor de mai sus. Datele de mai sus au arătat că TGs ar putea atenua semnificativ I/R-induse de leziuni cerebrale, dar PSs și OSs nu a putut.
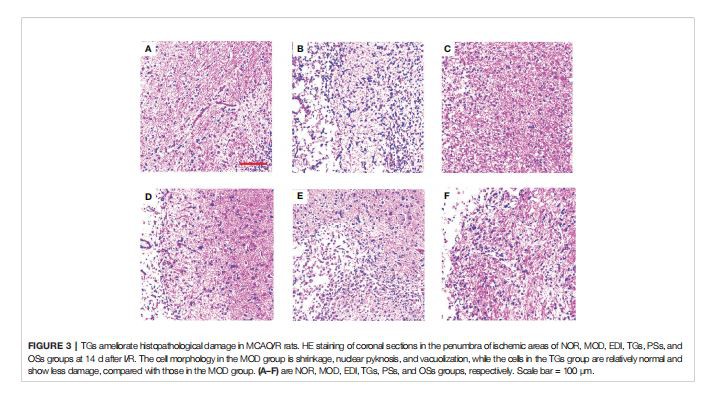
TGs ameliora daune histopatologice la șobolani MCAO/R
Pentru a determina unele dintre efectele TGs, PSs, și OSs tratament pe daune histopatologice, H & E colorare a fost făcut pentru a descoperi leziuni patologice. Structurile histomorfologice ale creierelor din grupul NOR au fost aranjate în mod regulat. Modificările morfologice din grupurile TGs au fost mai mici decât cele din grupul MOD. Cu toate acestea, grupurile de tratament PSs și OSs nu au prezentat o ameliorare semnificativă a modificărilor morfologice (Figura 3).
TGs atenua leziuni neuronale după I/R-induse de șobolani
Colorarea Nissl a arătat modificările histopatologice ale neuronilor din penumbra zonei ischemice. După cum se arată în figura 4, neuronii normali aveau un nucleol clar și o structură intactă. În grupul MOD, neuronii au mărit spațiile intercelulare. Corpurile nissl au fost dispărute, micșorate și pătate adânc. Cu toate acestea, aceste modificări au fost rareori observate în grupurile EDI, TGs și PSs. Aceste rezultate au ilustrat faptul că TGs și PSs ar putea atenua în mod semnificativ ischemie/reperfuzie induse de leziuni neuronale.
TGs atenuează întreruperea BBB după I/R-tratate șobolani
Testul albastru Evans este o metodă clasică pentru cercetarea schimbării permeabilității BBB. Rezultatele experimentului au arătat că a crescut Evans albastru a fost observat în grupul MOD, în timp ce a existat o scădere semnificativă Evans albastru în TGs și EDI-tratate șobolani. În plus, nu a existat nicio diferență semnificativă între grupurile de terapie PSs și OSS (Figura 5). Aceste rezultate au sugerat că TG-urile ar putea atenua în mod semnificativ perturbarea BBB.
TGs promova angiogeneza la I / R șobolani răniți
Studii mai recente arată că angiogeneza joacă un rol critic în recuperarea funcțională neurologică și rezultatul prognostic după accident vascular cerebral ischemic acut (Yuen et al., 2015). Pentru a evalua efectele TGs, PSs și OSs asupra angiogenezei, CD31 și a-SMA au fost utilizate pentru a cuantifica numerele capilare. Colorarea imunofluorescenței a arătat că grupul MOD a cauzat o scădere remarcabilă a expresiilor CD31 (Figurile 6A, B) și a-SMA (Figurile 6C, D) în penumbra zonelor ischemice ale șobolanilor I/R, în comparație cu șobolanii normali. Acest rezultat a ilustrat faptul că I /R ar putea provoca leziuni vasculare în cortexul penumbra emisferelor ischemice. Cu toate acestea, TGs și tratamentul EDI a crescut remarcabil densitatea capilară, angiogeneza și arteriogeneza, după cum indică expresiile crescute ale CD31 și a-SMA. Aceste rezultate sugerează că TGs ar putea promova angiogeneza în penumbra ischemică de șobolani I/R, dar PSs și OSs nu a putut.
TGs crește expresia proteinelor joncțiune strânsă în I /R șobolani răniți
Perturbarea BBB poate ridica conținutul de apă din creier și umflarea țesuturilor, ceea ce duce la leziuni cerebrale. Proteinele de joncțiune strânsă sunt componente structurale importante ale BBB (Tenreiro et al., 2016; Jiang et al., 2018). Pentru a testa dacă tratamentul TGs, PSs și OSs după accident vascular cerebral ar putea influența integritatea BBB, expresiile ZO-1, claudin-5 și ocludină au fost efectuate prin analiza imunofluorescenței. Rezultatele au indicat că expresiile claudin-5, ocludin și ZO-1 au scăzut vizibil în grupul MOD. Cu toate acestea, acestea au fost majorate substanțial după 14 zile de administrare a AG. Grupurile PS și OSs nu au prezentat modificări semnificative ale acestor expresii proteice (Figura 7). Aceste date au indicat că TGs poate reglementa expresii de proteine joncțiune strânsă și, probabil, menține integritatea BBB după I / R prejudiciu. TGs Creșterea pericite acoperire pe capilare în I / R rănit șobolani pericite acoperire pe capilare joacă un rol critic în menținerea integrității BBB (Armulik et al., 2010; Daneman et al., 2010). Astfel, am testat dacă acoperirea pericitelor ar putea fi crescută prin tratamentul TGs, PSs și OSs. Rezultatele analizei intensității imunofluorescenței au arătat că atât expresiile PDGFRb, cât și cele CD31 au scăzut dramatic în grupul MOD. Administrarea TG la șobolanii I/R a recuperat semnificativ sau chiar a crescut intensitățile de expresie ale PDGFRb și CD31, dar nu s-a observat nicio diferență în grupurile de tratament PSs și OSs (Figura 8). Astfel, tratamentul TGs ar putea crește semnificativ acoperirea pericitelor. Aceste constatări au confirmat, de asemenea, că TG-urile pot menține integritatea BBB după I/R.
TGs promova remodelarea neuronale în I / R șobolani răniți
Conform numeroaselor studii, neurogeneza după un accident vascular cerebral poate îmbunătăți semnificativ recuperarea funcțională (Grefkes and Ward, 2014; Zhang et al., 2019). Synaptophysin (SYN), densitate postsinaptică 95 (PSD-95) proteine, și microtubul-asociate proteine 2 (MAP-2) au fost folosite ca markeri pentru a examina plasticitatea neuronale în penumbra ischemică a cortexului. Pentru a evalua efectele tratamentului cu TGs, PSs și OSs asupra neurogenezei la șobolanii răniți I/R, s-au efectuat imunofluorescența și pata occidentală pentru expresiile SYN, PSD95 și MAP-2. După cum se arată în figurile 9 și 10, nivelurile de expresie SYN, PSD95 și MAP-2 la șobolanii I/R după 14 zile de reperfuzie au scăzut în comparație cu șobolanii NOR, în timp ce vindecarea TGs și PSs ar putea să-și regleze semnificativ nivelurile de expresie. Grupul de sisteme de operare nu a avut nicio schimbare semnificativă în comparație cu grupul MOD. Datele au indicat că TGs și PSs cura a fost capabil de a promova în mod dramatic remodelare neuronale după I / R prejudiciu.
TGs Alter Nrf-2 și Keap-1 Expresii în I / R șobolani răniți
Stresul oxidativ este un mecanism patogen principal în leziunile I/R (Ya et al., 2018; Yu et al., 2018). Studiile au verificat că Nrf-2 este un regulator principal al răspunsurilor antioxidative (Thompson et al., 2015). Pentru a investiga nrf-2 și Keap-1 mediate răspunsuri oxidative după I / R prejudiciu, am evaluat expresia citoplasmatică, precum și translocarea nucleară a Keap-1. Între timp, expresia Nrf-2 în țesuturile cerebrale ale șobolanului rănit I/R a fost, de asemenea, testată (figurile 10 și 11). Conform analizei imunofluorescenței, s-a constatat că Nrf-2 se află în principal la citoplasma din grupul NOR. În grupul TGs, expresia Nrf-2 în localizarea citoplasmatică a fost downregulated, dar upregulated în nucleu, și o expresie Keap-1 a scăzut, de asemenea, a fost observată. Datele au arătat că protecția creierului TGs ar putea fi asociată cu modularea Nrf-2 și Keap-1
TGs atenuatis țesutului cerebral stresul oxidativ în I/R șobolani răniți
Pentru a confirma efectele antioxidative ale TGs, activitățile SOD, CAT, GSH-Px și MDA au fost evaluate la șobolanii răniți I/R. În figura 12, conținutul de MDA a crescut semnificativ în grupul MOD și, în același timp, activitățile SOD, CAT și GSH-Px au scăzut, în comparație cu șobolanii normali. În schimb, tratamentul TGs a condus la o scădere semnificativă a conținutului de MDA și la o creștere a activităților SOD, CAT și GSH-Px. Aceste rezultate au confirmat în continuare activitatea antioxidare a TGs.

DISCUȚIE
Multe studii sugerează că TCMC. deserticolaare activități biologice extinse, de exemplu, îmbunătățirea capacității de a învăța, a memoriei și a imunității (Dong et al., 2007; Jiang și Tu, 2009; Wang et al., 2017; Xia et al., 2018). Cu toate acestea, componentele active ale C. deserticola pentru neuroprotecție rămân neclare. Lucrarea curentă are ca scop ecranarea componentelor active dinC. deserticolaîmpotriva accident vascular cerebral ischemic pe modelul MCAO /R. Trei extracte din C. deserticola (TGs, PSs, și sisteme de operare) au fost folosite pentru a evalua efectele lor asupra mcao/R șobolani, precum și mecanisme posibile.
Accidentul vascular cerebral este o boală cerebrovasculară acută comună. Studiile epidemiologice arată că accidentul vascular cerebral este mai frecvent la bărbați decât la femei (Sealy-Jefferson et al., 2012; Guzik și Bushnell, 2017). Astfel, în experimentul nostru, șobolanii de sex masculin au fost adoptați pentru teste. Rezultatele noastre au demonstrat că inducția I/R a accelerat stresul oxidativ și volumul infarctului, rupând BBB și ducând la leziuni nervoase și cerebrovasculare. După screening, TGs s-au dovedit a reduce volumul de infarct și de a promova remodelare neuronale și angiogeneza. În plus, s-a observat că agG-urile își mențin integritatea BBB după prejudiciul cauzat de I/R. Dimpotrivă, PS-urile și sistemele de operare nu aduc nicio atenuare semnificativă a prejudiciului I/R. Astfel, TG-urile sunt considerate principala fracțiune activă aC. deserticolapentru neuroprotecție, potențial prin promovarea remodelare neuronale, angiogeneza, și integritatea BBB prin activarea Nrf- 2/Keap-1 cale.
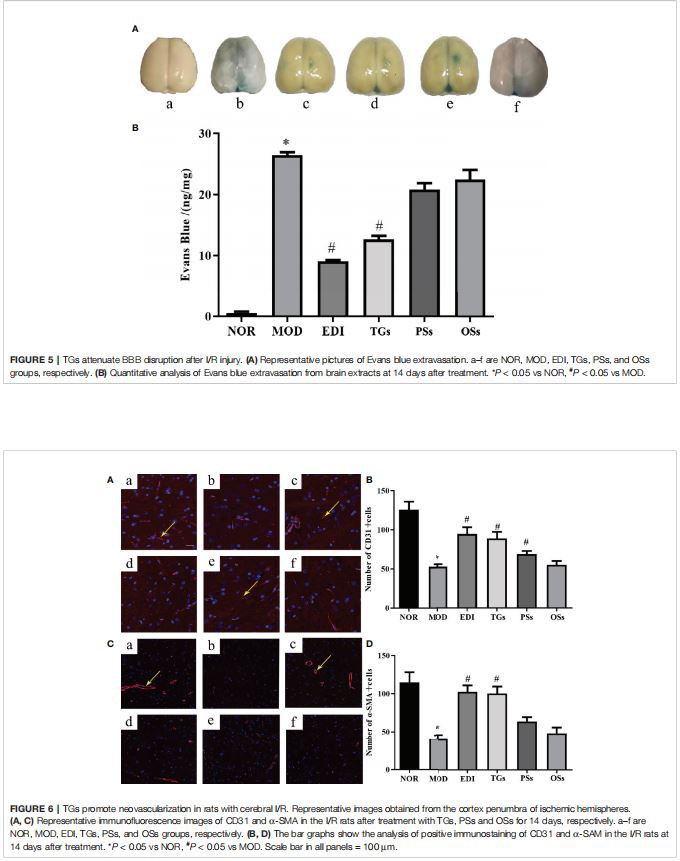
Dovezile de montare indică faptul că stabilirea unei circulații colaterale eficiente este semnificativ importantă pentru evitarea formării infarctului și a penumbrei ischemice și este un tratament critic într-un stadiu incipient al accidentului vascular cerebral ischemic (ElAli, 2016; Iwasawa et al., 2016). Proliferarea celulelor endoteliale vasculare și a celulelor musculare netede după infarctul ischemic determină stabilirea circulației colaterale. Cu toate acestea, modelele de ischemie au un fenomen comun - adică stresul oxidativ a existat pe scară largă în microvasculatura creierului. Datele studiului au arătat că un număr mare de antioxidanți pot perturba funcția BBB și proprietățile angiogenezei (Mentor și Fisher, 2017). CD31 și a-SMA sunt markerii celulelor endoteliale vasculare, precum și celulele musculare netede, respectiv (Saboor et al., 2016). Pentru a investiga efectul asupra proliferării celulare menționate mai sus a extractelor dinC. deserticola, Am examinat expresiile CD31 și a-SMA în omogenatul penumbrei ischemice cerebrale. Datele Curții au arătat că TG-urile au îmbunătățit în mod izbitor expresiile CD31 și a-SMA. Cu toate acestea, nu au existat diferențe semnificative pentru grupurile de sisteme de operare și sisteme de operare. Prin urmare, am dedus că TGs poate reduce leziuni ale creierului prin promovarea angiogeneza prin creșterea expresiilor de CD31 și a-SMA, în timp ce PSs și sisteme de operare nu a oferit nici o astfel de protecție împotriva leziuni ale creierului. Aceste rezultate au confirmat, de asemenea, că numai TGs ar putea preveni leziuni cerebrale I/R.
Accident vascular cerebral ischemic poate fi considerat ca urmare a ischemiei cerebrale cauzate de afectarea plasticității neuronale sau remodelarea zonelor creierului. Majoritatea pacienților cu accident vascular cerebral suferă deficite neurologice. Activarea neurogenezei este o strategie promițătoare pentru pacienții cu accident vascular cerebral pentru a-și îmbunătăți funcțiile neurologice (Cramer and Chopp, 2000). Neurogeneza participă direct la recuperarea funcției neurologice după leziuni cerebrale I/R (Zhang et al., 2019). Cercetările anterioare arată că TGs pot îmbunătăți rata de supraviețuire a celulelor piramidale hipocampale și pot induce neurogeneza (Lian et al., 2017). Stresul oxidativ provoacă pierderea neuronilor în timpul multor boli, cum ar fi Parkinson, accident vascular cerebral și așa mai departe (Duan și Si, 2019; Singh et al., 2019). Nrf-2 transcrie o mulțime de gene legate de neuroprotecție în regiunea lor promotor, în principal, inclusiv SOD, MDA, CAT, și ligaze gglutamyl cisteina, etc (Satoh et al., 2006). PROTEINELE SYN, PSD-95 și MAP-2, care sunt asociate îndeaproape cu formarea sinaptică și neurotransmisia, pot fi considerate markeri ai plasticității neuronale de cercetare în regiunea penumbrei ischemice. După ce am studiat, Curtea a constatat că vindecarea cu TGs ar putea crește semnificativ expresiile PSD95, SYN și MAP-2, indicând faptul că protecția cerebrală a TGs a fost corelată cu plasticitatea neuronală îmbunătățită în timpul I/R. Cu toate acestea, este păcat că nu există nici o diferență evidentă pentru PSs, precum și grupuri de sistem de operare. Aceste rezultate au indicat că TGs ar putea spori neuroplasticitate după leziuni cerebrale I/R.Cercetările imagistice asupra pacienților cu accident vascular cerebral au arătat că disfuncția BBB poate fi considerată un atribut izbitor al creierului periischemic (Bang et al., 2007). TJ-urile, care sunt compuse din proteine citoplasmatice, proteine transmembrane și molecule de aderență la joncțiune între celulele endoteliale capilare, sunt foarte importante în menținerea integrității BBB (Ye et al., 2019). Printre acestea, ZO-1, claudin-5 și ocludină sunt cele mai importante proteine din TJs. Dovezile de montare indică faptul că permeabilitatea crescută a BBB indusă de ischemie se corelează în general cu modificările ZO-1, claudin-5 și ocludin (Cao et al., 2016a; Page et al., 2016; Yu et al., 2017; Liu et al., 2018). În această lucrare, rezultatele au demonstrat că, deși TGs ar putea crește în mod semnificativ expresiile ZO-1, claudin-5 și proteine ocludin în țesuturile cerebrale induse de MCAO, nici PSs, nici OSs nu au făcut-o. BBB constă din celule endoteliale cerebrale și este strâns asociat cu pericite (Nyul-Toth et al., 2016). Pericitele sunt vitale pentru integritatea BBB (Bell et al., 2010). Accidentul vascular cerebral ischemic declanseaza moartea pericitelor si detasarea de celulele endoteliale cerebrale in faza acuta, destabilizand astfel microvasculatura si modificand proprietatile BBB (Zaharia et al., 2013). Datele curții au arătat că TG-urile ar putea crește acoperirea pericitelor pe capilare și ar putea crește nivelurile de expresie ale ZO-1, claudin-5 și ocludin. Aceste fenomene au demonstrat că TGs ar putea proteja în mod eficient integritatea BBB după leziuni cerebrale I/R. În rezumat, TGs poate atenua leziuni cerebrale în mai multe moduri, cum ar fi promovarea angiogeneza, îmbunătățirea plasticitatea neuronale, și menținerea integrității BBB.

Am investigat apoi calea de semnalizare pentru a explora mecanismul care stă la baza protecției creierului TGs. Procesul de rănire I/R este multifactorial și, prin urmare, numeroase mecanisme sunt implicate în patogeneză. Stresul oxidativ este un factor de risc fundamental care contribuie la leziunile cerebrale induse de I/R (Suda et al., 2013), cum ar fi deteriorarea structurii BBB, disfuncția endotelială vasculară și agravarea leziunilor neuronale ischemice (Xiong et al., 2015; Caglayan et al., 2019; Priestley et al., 2019). Astfel, stresul oxidativ a devenit o țintă terapeutică atractivă în leziunile cerebrale induse de I/R. Enzimele de fază 2, care sunt mediate de factorul nuclear E2-2 (Nrf-2), au fost considerate un mijloc important prin care neuronii se protejează împotriva stresului oxidativ (Suzuki și Yamamoto, 2015; Ya et al., 2018). Dovezile de montare indică faptul că activarea Nrf-2 în timpul I/R este o țintă terapeutică potențială pentru neuroprotecție (Ding et al., 2015; Zhang R. et al., 2017). Nrf-2, ca un important regulator al apărării antioxidante endogene, mediază nivelul de hem oxigenază 1 (HO-1) și alte enzime antioxidante, cum ar fi NAD(P)H chinonă oxidoreductază 1 (NQO1), SOD, CAT, GSH și MDA (Siow et al., 2007; Ding et al., 2014). În plus, Nrf-2 joacă un rol important de reglementare în angiogeneză. Studiul de față arată că Nrf-2 poate fi îmbunătățit și activat în mod semnificativ în procesul de dezvoltare vasculară (Wei et al., 2013).
Așa cum s-a descris anterior (Jiang și Tu, 2009), TGs conțin o mulțime de compuși bioactivi, de exemplu, echinacozidă, tubulozidă A, acteosidă, izo-acteozidă și 2'-acetilacteozidă, iar unele dintre ele au prezentat funcții neuroprotectoare după leziuni cerebrale I/R (Peng et al., 2016). Echinacozidul are o mulțime de efecte farmacologice, cum ar fi antioxidarea, anti-senescența, neuroprotecția, anti-inflamația, promovarea cicatrizării, hepatoprotecția, promovarea formării osoase și activitățile anti-tumorale (Yu et al., 2016; Li et al., 2018; Zhang Y. et al., 2018; Ji et al., 2019; Xu et al., 2019). Recent, echinacozidul a fost identificat ca un antioxidant puternic în sistemul nervos central (Lu et al., 2016). Echinacozidul poate reduce conținutul de MDA și poate îmbunătăți activitățile SOD și GSHPx în leziunile cerebrale ale ischemiei, iar analiza moleculară de andocare a arătat că echinacozidul se poate lega de Keap-1, ceea ce duce la translocarea nucleară Nrf-2 (Li et al., 2018). Studiul Xia a arătat că acteosidul ar putea reduce volumul infarctului și conținutul de apă din creier pentru a îmbunătăți deficitele neurologice la șobolanii MCAO/R prin atenuarea stresului oxidativ (Xia et al., 2018). Alte studii au demonstrat că izo-acteosidul ar putea crește activitățile enzimelor antioxidante celulare, SOD și CAT în celulele V79-4 tratate cu H2O2 (Chae et al., 2005). Pe baza rapoartelor de mai sus ale compușilor activi conținute în TGs, este posibil să se deducă că TGs ar putea proteja împotriva accident vascular cerebral ischemic prin căile de antioxidare.
Li a raportat cu privire la efectele neuroprotectoare ale glicozidelor feniletanoide (PHG) asupra apoptozei induse de H2O2 asupra celulelor PC12 prin calea Nrf2/ARE (Li et al., 2018). Aceste PHG-uri au fost suprimate semnificativ prin declanșarea translocației nucleare Nrf2 și creșterea expresiilor ho-1, NQO1, subunitatea ligasecatalitică glutamat-cisteină (GCLC) și subunitatea modificator de liga glutamat-cisteină (GCLM) (Li et al., 2018; Gong et al., 2019). Prin urmare, aceste constatări sugerează că calea Nrf-2/ARE joacă un rol crucial în efectele protectoare mediate de PHG asupra celulelor neuronale. În mod similar, în cadrul acestui studiu, Curtea a constatat că AG ar putea reduce nivelul de MDA și ar putea crește nivelurile de SOD, CAT și GSH-Px la șobolanii I/R. Între timp, TGs ar putea upregulate expresia Nrf2 în nucleu, downregulate expresia corespunzătoare în citoplasma, și reduce semnificativ expresia Keap-1. Prin urmare, calea Nrf-2/Keap-1 pot fi implicate în TGsmediated efecte neuroprotectoare. Validarea în continuare a acestei căi ar fi efectuată cultura de celule in vitro cu privarea de oxigen-glucoză / modele de prejudiciu reoxygenation în viitor. Mai mult decât atât,C. deserticolaextractele au fost administrate în studiul nostru timp de 14 zile continuu. Deoarece neurogeneza adultă ar afecta interpretarea efectelor neuroprotectoare în timpul 14 zile de reperfuzie, neurogeneza nu poate fi exclusă în proiectarea experimentului nostru actual în explorarea efectului neuroprotector al CT-urilor. Aceasta este limitarea cercetării noastre.
În concluzie, TG-urile sunt de laC. deserticolacare pot spori angiogeneza si neurogeneza, precum și să mențină integritatea BBB în I/R șobolani prejudiciu, dar nu PSs și OSs. Efectele ar putea fi mediate prin activarea căii Nrf-2/Keap-1.


